编者按
2026年3月21日,第一届长三角心血管代谢管理多学科学术会议在上海复旦大学附属华山医院成功举办。会议围绕心血管代谢领域的最新研究进展、临床实践中的争议问题及未来发展方向展开深入探讨与交流,为与会同道呈现了一场多学科交融的学术盛宴。会议期间,复旦大学附属中山医院葛均波院士团队孙爱军教授基于基础和临床研究数据,分享了团队在糖脂代谢之外的炎症、线粒体功能、自噬等通路方面的研究成果和心肌保护的潜在新靶点;提出,心血管代谢疾病的复杂性要求我们积极进一步探索多靶点联合干预新策略,以期更好的改善患者预后。

一
线粒体ALDH2:心力衰竭防治的关键靶点
根据国家心血管病中心《中国心血管健康与疾病报告2024》,心血管疾病(CVD)位列我国居民死亡构成比首位(图1)[1]。心脏病学领域的权威——哈佛大学医学院E.Braunwald教授曾直言“心力衰竭(HF)是21世纪心血管疾病的最后战场”。据预测,到2035年我国HF患者将达2270万人,累计经济损失预计超过10 011亿国际元,占同期GDP的0.26%[2]。在人口老龄化及代谢疾病的双重压力下,我国HF防控形势日益严峻。
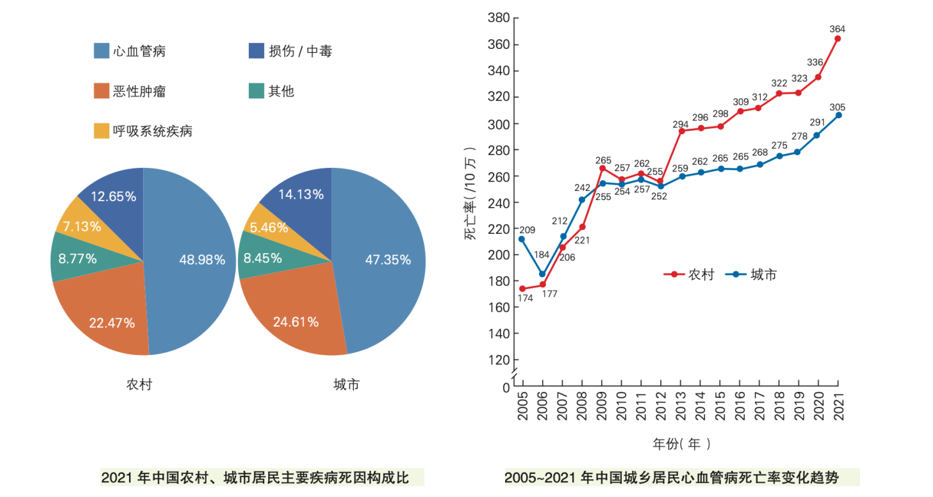
图1. 我国CVD死亡构成比及变化趋势
心脏发挥“泵”功能需要强大的供能系统,心肌细胞中约三分之一的体积由线粒体占据。当线粒体因各种原因受损时,线粒体自噬、能量代谢紊乱及氧化应激等一系列病理过程会被激活,最终可能导致心力衰竭的发生与发展[3~6]。乙醛脱氢酶2(ALDH2)是线粒体内一种重要的醛类代谢酶,具有脱氢酶和酯酶双重活性。在衰竭心肌的线粒体中,ALDH2的表达显著下调[7];线粒体ALDH2基因突变是心衰的高危因素,会引起心脏能量代谢紊乱,影响心脏的舒张功能[8]。
二
中性粒细胞NETosis:心肌缺血再灌注损伤的新机制
1
ALDH2缺失通过NETosis加重心肌损伤
中性粒细胞胞外诱捕网(NETs)的形成过程(NETosis)是近年来免疫学研究的热点。NETosis指中性粒细胞在活化状态下释放染色质DNA和颗粒蛋白形成网状结构的过程,它在抗感染免疫中发挥重要作用,但过度激活也会导致组织损伤。研究表明,ALDH2 rs671多态性与NETosis的易感性密切相关[9]。ALDH2缺失可通过增强NETosis加重心肌缺血/再灌注(I/R)损伤,这一发现为理解心肌I/R损伤的免疫机制提供了新视角。
2
孟鲁司特:老药新用的转化突破
孙爱军教授团队的研究显示,MPO-DNA与白三烯C4(LTC4)水平可作为预测直接经皮冠状动脉介入治疗(pPCI)术后ST段抬高型心肌梗死(STEMI)患者不良预后的血清标志物;而靶向NETosis及使用LTC4受体拮抗剂,是改善心肌缺血再灌注损伤(I/RI)颇具前景的治疗手段(图2)[10]。对此,德国海德堡大学曼海姆医学院心血管病中心主任Stellos教授撰文给予高度评价,指出该研究为靶向NETosis的治疗策略提供了新思路,强调在心血管疾病的个性化与精准化治疗中需考量患者遗传背景的重要性,并提出可将抗哮喘药物应用于减轻心肌缺血再灌注损伤。
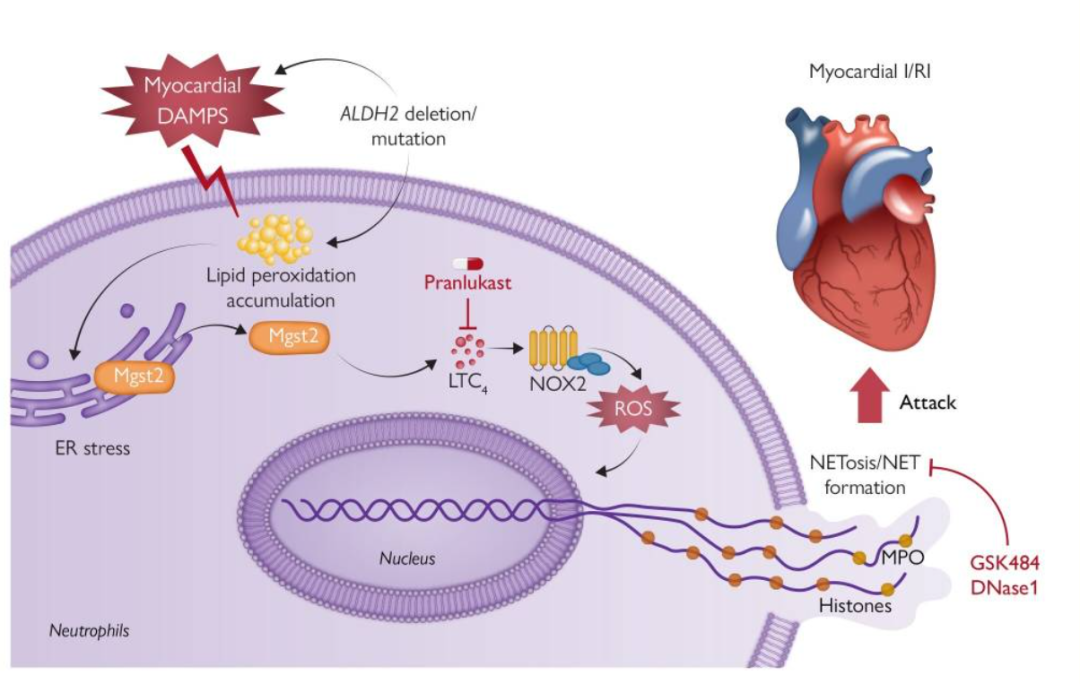
图2. ALDH2缺陷、中性粒细胞NETosis与心肌缺血再灌注损伤的机制通路
孟鲁司特是一类白三烯受体拮抗剂,长期用于哮喘和过敏性鼻炎的治疗,安全性良好;已有两项机制研究发现其在急性心肌梗死后预防心脏病理性重构和心力衰竭方面具有应用价值[11,12]。目前,孙爱军教授团队已设计多中心、随机、对照、双盲、平行组研究,探究孟鲁司特能否降低接受pPCI的STEMI患者术后病理性左室重构的发生率,推动这一老药向心梗治疗领域的临床转化。
三
硫辛酸:缺血性心衰代谢调控的临床探索
1
机制研究基础
α-硫辛酸(α-LA)是一种强效抗氧化剂,具有清除自由基、螯合金属离子及再生维生素C、维生素E、谷胱甘肽等其他抗氧化剂的多种生物学活性。前期动物研究显示,α-LA可显著减轻主动脉缩窄(TAC)诱导的野生型小鼠左心室肥大、纤维化及功能障碍,但对ALDH2敲除小鼠无此保护作用,提示ALDH2是硫辛酸发挥心肌保护效应的必要介质。进一步机制研究表明,α-LA通过恢复ALDH2的活性与表达,上调线粒体自噬受体蛋白FUNDC1的水平,从而发挥心肌保护作用。FUNDC1是介导缺氧诱导线粒体自噬的关键受体分子,其表达上调可促进损伤线粒体的清除,维持线粒体质量稳态。这一分子机制涉及ALDH2-Nrf1-FUNDC1信号级联的激活,为硫辛酸的心肌保护作用提供了理论依据(图3)[13]。
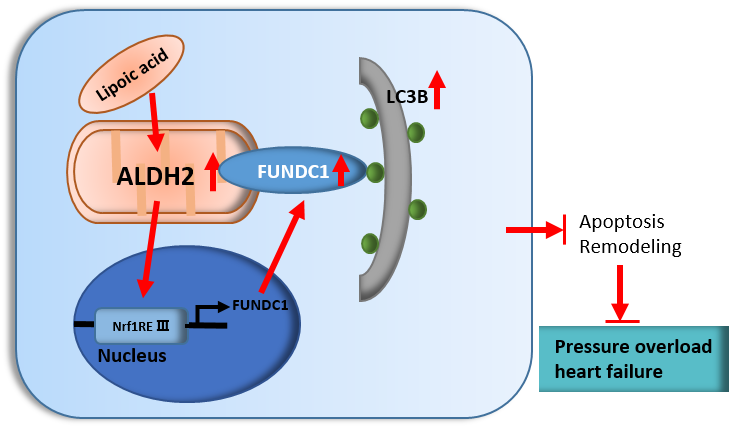
图3. α-LA通过激活ALDH2-Nrf1-FUNDC1信号级联发挥保护作用
2
临床研究设计与结果
为验证前期机制研究的临床转化价值,孙爱军教授团队于2019~2023年开展随机对照研究,在国内4家医疗中心筛选398例缺血性心衰(IHF)患者,最终入组300例并随机分组,进行2年药物干预和临床随访。尽管受新冠疫情影响,仍有277例患者纳入最终分析。结果显示,在主要终点方面,硫辛酸未显著降低IHF患者2年期全因死亡率或因心衰再住院率(HR=0.753,P=0.231);但在次要终点方面表现出显著获益:硫辛酸可显著改善患者左室射血分数(LVEF提高约3%,P=0.002),6分钟步行距离改善约30米(P=0.008);亚组分析显示一致的临床获益趋势,且安全性良好[14]。该研究证实了硫辛酸对缺血性心衰患者心功能和运动能力(LVEF和6MWD)的改善作用,表明靶向ALDH2的治疗策略具备良好的转化前景。目前,孙爱军教授团队正联合国内11家单位开展更大规模的多中心临床研究以验证相关结论。
四
ALDH2突变的其他影响
1
ALDH2是否在血小板活化、
血栓形成中发挥作用?
全球约8%的人群携带ALDH2 rs671突变,该突变在亚洲人群中尤为常见。研究发现,ALDH2突变者卒中、心梗等动脉血栓事件的发生率显著增加。血小板活化是动脉血栓形成的关键环节,抗血小板治疗也是目前防治动脉血栓形成的重要手段。动脉内皮损伤暴露内皮下胶原和vWF,触发血小板黏附过程;血小板黏附后可放大自身活化信号,诱导整合素αIIbβ3活化,进而导致血小板聚集、动脉血栓形成,引起组织器官缺血。
然而,研究发现即使接受双联抗血小板治疗,携带该突变的冠心病患者血小板对胶原(collagen)的反应性仍显著增加,但对凝血酶(thrombin)和ADP诱导的血小板聚集无显著影响。进一步研究揭示,ALDH2缺失通过干扰线粒体复合体I(complex I)的组装及功能,增强collagen/GPVI/NOX1途径诱导的活性氧(ROS)合成及血小板活化。更为重要的是,补充酰胺腺嘌呤二核苷酸(NAD+)可拮抗ALDH2 rs671突变导致的血小板高反应性及血栓高风险,为携带该突变人群的心血管风险干预提供了新思路(图4)[15]。
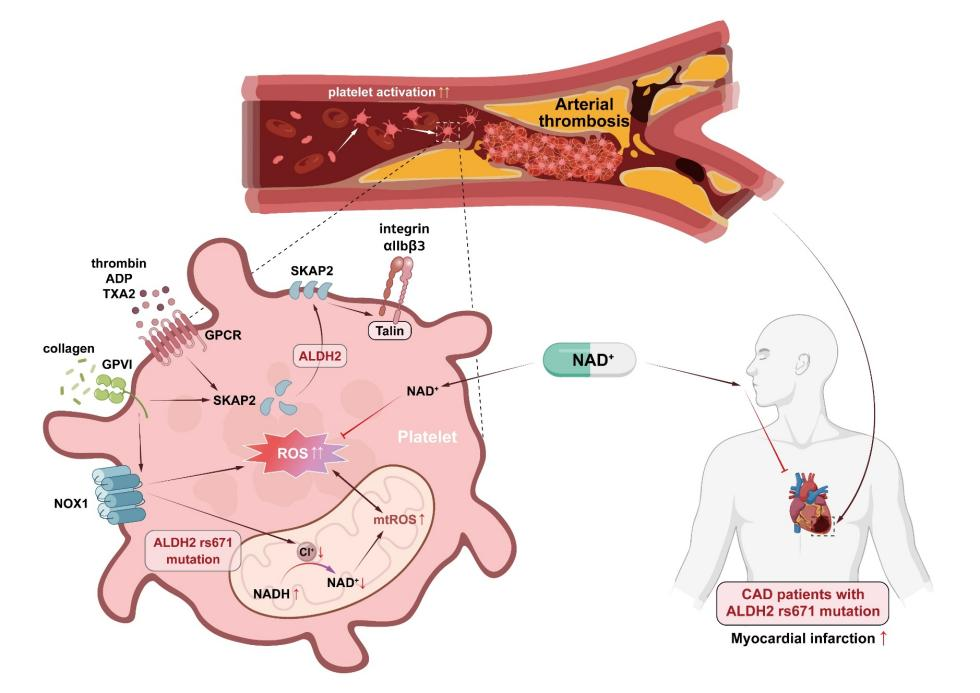
图4. 补充NAD+可拮抗ALDH2 rs671突变导致的血小板高反应性及血栓形成
2
高原低氧适应与心肌保护
随着我国西部大开发和高原旅游业的蓬勃发展,赴高原地区工作和旅行的人群日益增多。研究发现,ALDH2全身敲除小鼠在高原低氧环境下死亡率显著增加(高达85%),心功能损伤明显加重。高原低氧环境下心肌细胞ALDH2活性和表达降低,削弱了对脂质过氧化物4-HNE的清除能力,导致ROS产生生成增多;同时激活PPARs/CPT1通路,促进脂肪酸转运并增加线粒体内脂肪酸沉积,引发脂毒性损伤,进而加剧线粒体功能紊乱与心肌损伤[16]。
孙爱军教授团队已获两项发明专利:“一种与高原低氧耐受适应性相关的多态性位点及其应用”和“CPT1抑制剂在制备防控高原病药物中的应用”。目前,团队正与转化彩章科技、西藏旅投合作推进高原健康文旅项目,为援藏人员、驻边官兵及高原旅居人群提供新型干预策略。
五
其他研究进展:多维度探索心肌保护
1
靶向抑制TBK1和CD38预防阿霉素心脏毒性
cGAS-STING信号通路在阿霉素心脏毒性中发挥关键作用——其通过CD38调控内皮细胞与心肌细胞NAD+水平下降,进而影响线粒体功能。靶向抑制TBK1和CD38可有效预防阿霉素心脏毒性,同时保障阿霉素的抗肿瘤效果[17]。
2
心脏损伤早期诊断标记物:
GSDMD标志物
缺氧复氧诱导心肌细胞焦亡是通过Caspase11激活GSDMD通路实现的,研究进一步证实心肌细胞焦亡后GSDMD可释放入外周血,有望作为心脏缺血再灌注损伤的早期诊断标记物[18]。
3
组胺代谢与心衰(HF)
组胺N-甲基转移酶(HNMT)是心衰进展的关键靶点,其通过消耗S-腺苷甲硫氨酸(SAM)调控H3K27me3修饰的表观遗传机制,构成了连接心脏代谢与表观遗传的重要桥梁。临床转化方面,抗疟疾药物阿莫地喹具有治疗心衰的潜力,尿液中的N-甲基组胺可作为心衰标志物[19]。对此,苏黎世大学心脏病学系Francesco Paneni教授评价道:“这是一项重要研究,揭示了一种新的信号机制及潜在药物靶点,可用于调节衰竭心脏中的SAM水平与表观遗传重塑。”
4
运动改善心衰的表观遗传机制
运动可通过表观遗传途径改善心衰患者的心功能及葡萄糖摄取能力。小动物PET-CT显示,运动能增加衰竭心脏对葡萄糖的摄取;透射电镜结果表明,运动后心衰心脏的线粒体结构得到改善。基于这一发现,孙爱军教授团队获得“HDAC4抑制剂在制备治疗心衰药物中的应用”国家发明专利授权。
结语
围绕线粒体ALDH2这一核心靶点,孙爱军教授团队从糖脂代谢之外的全新视角开展系列研究,系统阐明了心肌保护的新机制,充分体现了“从临床中来,到临床中去”的转化医学理念。研究始终聚焦心血管疾病的重大临床问题,从NETosis到代谢调控、从血小板活化到高原适应、从组胺代谢到表观遗传,深入探索分子机制并积极推进转化应用,为心血管疾病的精准防治提供了丰富的理论依据和潜在干预靶点。
专家简介
孙爱军教授
复旦大学附属中山医院
长期从事心力衰竭和能量代谢研究及转化工作,担任上海市心血管临床医学中心副主任,复旦大学中山医院临床医学研究院副院长,心研所实验室主任,国家卫健委缺血性心脏病重点实验室主任。
主持国家重点研发及基金委重点、杰青等多个项目,以通讯或第一作者在Eur Heart J、Circulation、PNAS等发表SCI论文120余篇,部分被写入国内外指南或专家共识。获国家发明或实用新型专利20余项,部分实现了临床转化。
担任Vessel Plus主编和7个国际期刊编委,多个国家及省部级重点实验室学术委员会委员,获多项科技成果奖。
参考文献:
2.Wang H, . Yang J. Eur Heart J, 2025
3.Schwartz et al. Circulation. 2019;140:1205–1216
4.Sciarretta et al. Annu Rev Physiol. 2018;80:1-26
5.Münzel T et al. J Am Coll Cardiol. 2017;70:212-229
6.Nicola-A vila et al. Cell. 2020, 183, 1–16
7.徐丹令,孙爱军,葛均波.中国病理生理杂志,2006.
8.Wang C, .Sun A, Ge J. J Mol Med. 2016.
9.Nicoletta Sorvillo,et al. Circ Res. 2019
10.Yang K,.GuoY, Ge J, Sun A. Eur Heart J.2024
11.Ulrich M Becher et al. J Mol Cell Cardiol. 2011.
12.Majeda Muluhie et al. Sci Rep. 2024.
13.Li W, . Sun A, Ge J. Cell Death & Disease. 2020.
14.Chen H, Ge J, Sun A. JACC: Heart Failure, 2025.
15.Zhong H, Sun A, Ge J. Cardiovascular Res. 2025.
16.Gao R, Ge J, Sun A. TRANSL RES. 2024.
17.Luo W, Sun A, Ge J. Circ Res. 2023.
18.HR Shi, AJ Sun, JB Ge. Cir Res, 2021.
19.Zhang J, Yang J, Ge J, Sun A. Eur Heart J. 2026.


我要留言