编者按:代谢功能障碍相关脂肪性肝炎(MASH)药物研发正步入新纪元,多种靶向不同机制的药物在临床试验中展现出潜力。然而,由于缺乏直接的头对头比较研究,如何评估这些药物的相对疗效已成为临床决策的难点。近期发表于Hepatology的一项系统综述和网络Meta分析,通过对现有随机对照试验(RCT)的综合评估,为不同药物在关键组织学终点上的疗效提供了清晰的排序证据,这对指导临床实践及未来研究具有重要价值。

研究背景:MASH治疗的挑战与机遇
MASH是与全球肥胖和糖尿病流行密切相关的慢性肝病,影响着全球近三分之一的人口。该病是驱动肝纤维化、肝硬化、肝功能失代偿乃至肝细胞癌的关键因素,构成了严峻的公共卫生挑战。MASH的病理生理机制极为复杂,涉及胰岛素抵抗、脂毒性、氧化应激、炎症反应和纤维化信号通路等多环节的相互作用。其中,肝纤维化是决定MASH患者长期临床预后的核心病理特征——纤维化分期越高,肝脏相关并发症及死亡风险越呈急剧上升趋势。因此,逆转或延缓肝纤维化进程已成为MASH药物研发的首要目标。
在生活方式干预之外,MASH领域长期面临无有效获批药物的治疗空白期,临床管理主要依赖生活方式干预,但患者依从性及疗效持久性均面临严峻挑战。近年来,随着对MASH发病机制认知的深入,针对成纤维细胞生长因子21(FGF21)通路、胰高糖素样肽-1(GLP-1)受体、甲状腺激素受体-β(THR-β)等多个靶点的药物研发已取得突破性进展。多项II期和III期临床试验显示,这些新药在改善肝脏组织学方面展现出令人鼓舞的疗效。然而,这些试验大多采用安慰剂对照设计,缺乏药物间的直接比较数据,使得临床医生难以在众多选择中为特定患者做出最优决策。
研究设计:网络Meta分析与主要终点
为破解缺乏头对头研究证据的困境,本研究采用严谨的系统综述与网络Meta分析(NMA)方法。研究团队严格遵循PRISMA声明规范,系统检索了PubMed及Embase数据库,纳入2020年1月1日至2024年12月1日期间发表的、针对活检证实MASH患者的Ⅱ-Ⅳ期随机对照试验(RCTs)。分析采用贝叶斯统计框架,通过间接比较评估缺乏直接对照证据的多种药物疗效差异,并运用累积排名概率曲线下面积(SUCRA)对各种药物的疗效排序——SUCRA值越高表明疗效越优。
研究设定了两个协同主要终点,均基于肝脏组织学评估:(1)肝纤维化改善≥1期且MASH未恶化;(2)MASH缓解且肝纤维化未恶化。这两个终点指标是当前MASH新药临床试验中普遍采用的关键疗效指标。
研究结果:MASH药物疗效的全面图景
经过严格筛选,该研究最终纳入29项独立的RCTs、9324例经活检证实的MASH患者。其中,9项于北美开展,3项在亚洲,1项在欧洲,其余16项为跨国研究,且绝大多数(93.1%)为多中心试验。受试者基线特征显示其代表典型MASH人群,多数伴有显著肝纤维化。
为清晰呈现药物间比较关系,研究构建了网络关系图(图1)。该图通过节点大小直观反映患者分配数量,边粗细则对应的数量,从而系统体现各药物间的证据连接强度。
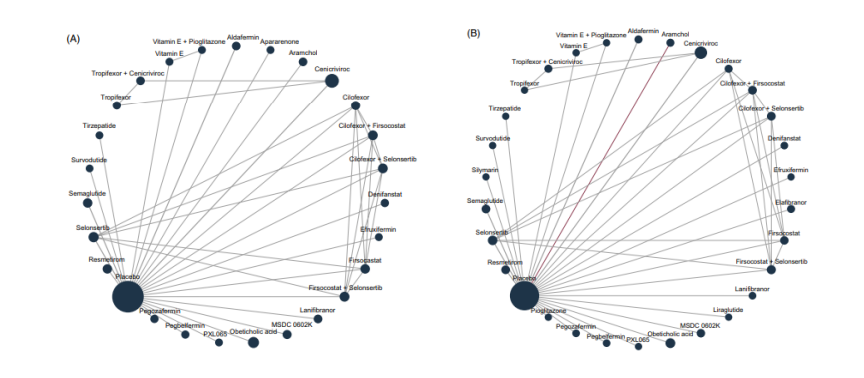
图1. 纳入研究的网络关系图
(A)肝纤维化改善≥1期且MASH未恶化、(B)MASH缓解且肝纤维化未恶化
协同主要终点一:肝纤维化逆转
在“肝纤维化改善≥1期且MASH未恶化”这一主要终点评估中,共纳入24项RCTs、共8708例患者,结果揭示了不同药物在逆转肝纤维化方面的疗效差异(图1)。单药治疗中,FGF21类似物Pegozafermin疗效最优,其SUCRA值高达79.92,相对风险(RR)为3.46(95%置信区间[CI]:1.54~11.15);脂肪酸合酶(FASN)抑制剂Denifanstat的SUCRA值60.64;葡萄糖依赖性促胰岛素多肽和胰高糖素样肽-1(GIP/GLP-1)双受体激动剂Survodutide的SUCRA值59.89;FXR激动剂奥贝胆酸(Obeticholic acid)的SUCRA值58.86;GIP/GLP-1双受体激动剂替尔泊肽(Tirzepatide)的SUCRA值57.37;THR-β激动剂Resmetirom的SUCRA值50.14,均显示出较好的纤维化改善潜力。
联合疗法表现亮眼:法尼醇X受体(FXR)激动剂Cilofexor联合乙酰辅酶A羧化酶(ACC)抑制剂Firsocostat的SUCRA为71.38,紧随单药FGF21类似物Pegozafermin之后;Cilofexor联合凋亡信号调节激酶1(ASK1)抑制剂Selonsertib的SUCRA值达69.11,位列第三。
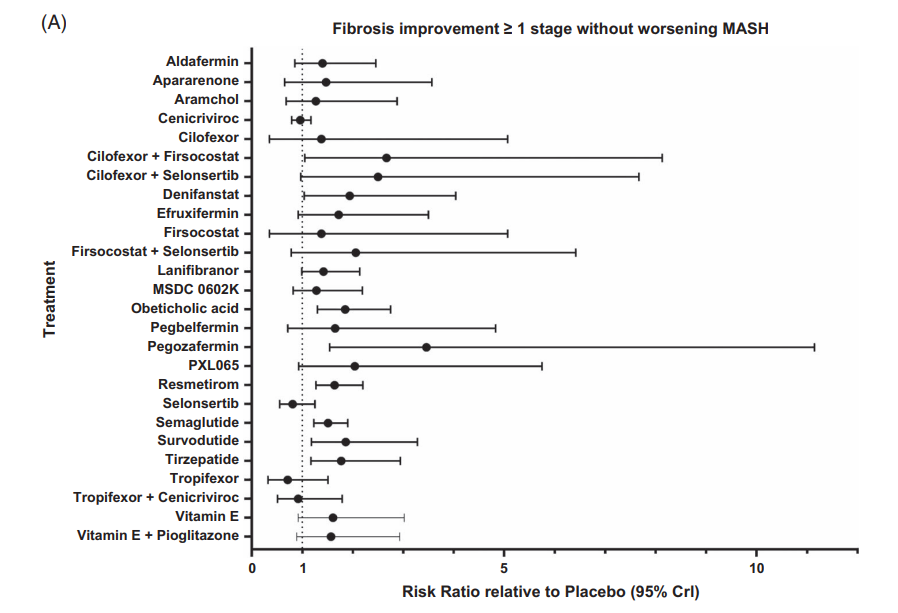
图1:不同药物在“纤维化改善≥1期且MASH不恶化”终点的治疗效果森林图
协同主要终点二:MASH缓解
在“MASH缓解且肝纤维化未恶化”这一主要终点评估中,纳入28项RCTs、9277例患者,结果揭示了不同药物的疗效差异(图2)。
FGF21类似物Pegozafermin以最高SUCRA值(94.32)位居榜首,其相对风险(RR)达8.65(95%CI:2.63~59.42);GIP/GLP-1双受体激动剂Survodutide、替尔泊肽紧随其后,SUCRA分别为90.87、84.70,RR值分别为6.62(95%CI:3.13~17.97)、4.65(95% CI:2.31~10.66)。其次,FGF21类似物Efruxifermin的SUCRA为76.22、GLP-1受体激动剂利拉鲁肽的SUCRA为71.58,THR-β激动剂Resmetirom的SUCRA为63.95。这些数据进一步验证了靶向代谢通路——特别是FGF21信号通路与多重肠促胰素受体激动剂——在实现MASH病理学缓解中的核心作用,为临床治疗策略的选择提供了高水平的循证医学证据。
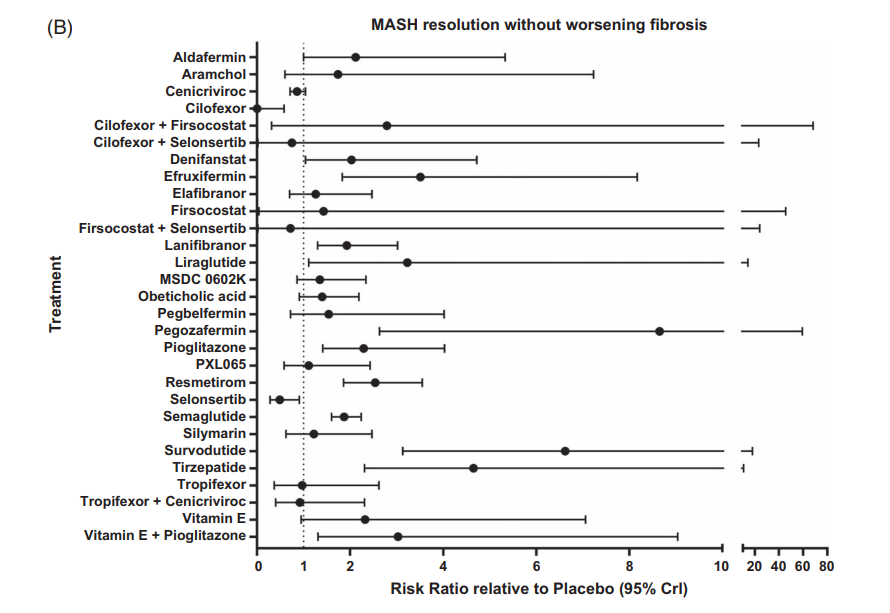
图2:不同药物在“MASH缓解且纤维化不恶化”终点的治疗效果森林图
此外,在2个共同主要终点的SUCRAs二维分布中,Pegozafermin、Cilofexor+Firsocostat、Survodutide等均处于较高水平,综合疗效表现突出(图3)。
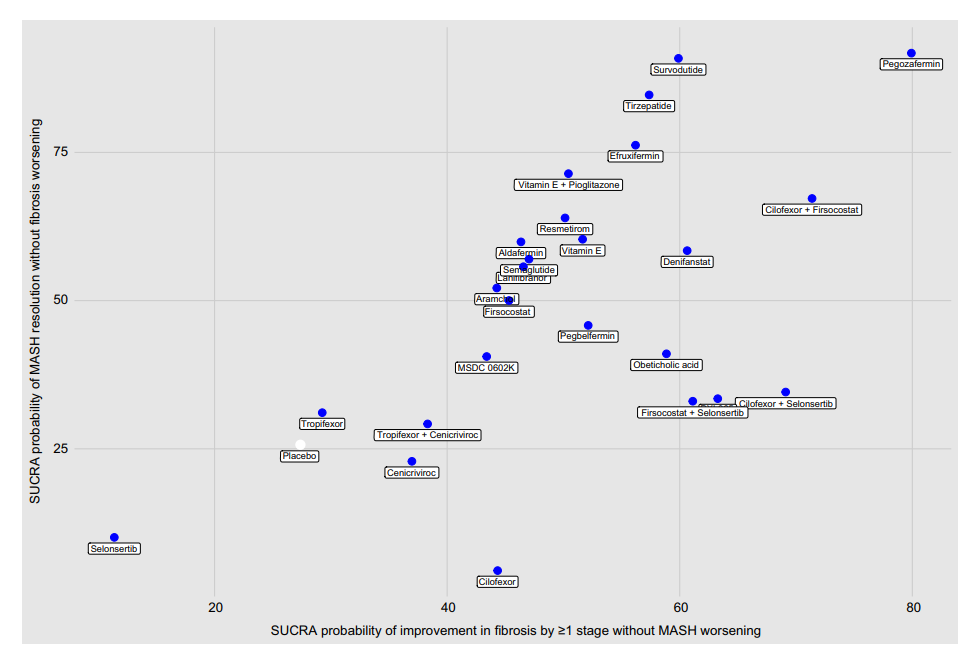
图3. 各药物在两大协同主要终点上的SUCRA二维图
亚组分析:治疗时长与作用机制的影响
为验证疗效排序的稳健性,研究者开展了基于治疗时长的敏感性分析,揭示了治疗周期对药物疗效评估的关键影响。结果显示,当治疗时长≥52周时,在“肝纤维化改善≥1期且MASH未恶化”的终点中,FASN抑制剂Denifanstat以SUCRA值66.49跃居首位,FXR激动剂奥贝胆酸以65.90紧随其后,GIP/GLP-1受体激动剂替尔泊肽则以62.98位列第三,提示这些药物在长期治疗中可能具有更持久的纤维化逆转效果。在“MASH缓解且肝纤维化未恶化”终点中,替尔泊肽以87.03的SUCRA值展现绝对优势,进一步验证了其作为长效治疗方案的潜力。而在治疗周期<52周的试验中,Pegozafermin在纤维化改善(SUCRA:65.92)和MASH缓解(SUCRA:84.09)两个终点上均排名第一,显示出其快速起效的特性。
本项敏感性分析强调了临床试验设计中治疗时长选择的重要性,表明不同药物可能具有不同的起效速度和作用模式,为临床根据患者情况选择短期或长期治疗方案提供了线索。从作用机制上看,FGF21类似物和GLP-1受体相关激动剂在两个终点上均表现出强大的竞争力,而THR-β激动剂瑞则展现了均衡且稳健的疗效。这些发现为理解不同药物的作用特点及未来探索联合用药提供了重要洞见。
研究局限性
本研究亦需谨慎考量以下局限性:首先,药物间疗效比较主要基于间接证据网络,缺乏头对头直接对照试验的验证,可能存在选择偏倚或混杂因素干扰;其次,纳入研究在试验设计(如随机方法、盲法实施)、基线人群特征(如肝纤维化分期分布、代谢合并症比例)及终点判定标准等方面存在显著异质性,可能影响结果的外推性;最后,部分药物仍处于早期研发阶段(如Ⅰ/Ⅱ期临床试验),其长期安全性数据尚未完全明确,且最终能否通过监管审批存在不确定性。因此,对结果的解读需保持谨慎。
结语
本项网络Meta分析为MASH药物治疗领域提供了迄今最全面的疗效排序证据,对临床实践和未来研究具有重要的指导意义。研究结果清晰地揭示了Pegozafermin、Survodutide和替尔泊肽为代表的新型药物在改善肝脏组织学方面的巨大潜力。这些数据不仅有助于指导未来临床试验的设计,特别是在联合治疗方案的探索上,也为临床医生在多种治疗选择并存时进行个体化决策提供了参考。未来,亟需开展更多头对头的RCT来直接验证这些发现,并推动非侵入性诊断工具的开发,以期为MASH患者带来更有效、更安全的治疗策略。
参考文献:
Souza M, et al. Comparison of pharmacological therapies in metabolic dysfunction–associated steatohepatitis for fibrosis regression and MASH resolution: Systematic review and network meta-analysis. Hepatology. 2025;82:1523-1533.
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。



我要留言