编者按:
高血压的管理正从“单纯降压”迈向“精准分型治疗、靶器官保护”的新纪元。长期以来,高血压被视为血流动力学异常(如心脏泵血、血管阻力)所致,而现代医学研究已彻底更新这一认知:慢性低度炎症贯穿高血压发生、发展及靶器官损害的全过程,是核心驱动因素。在中华医学会第二十四次介入心脏病学论坛上,首都医科大学附属北京朝阳医院钟久昌教授带来题为《炎症与高血压发病机制研究进展》的精彩演讲,系统揭示了从免疫细胞失衡、炎症因子释放到RAAS/交感神经系统激活恶性循环,再到肠道菌群调控、靶向铜死亡信号及抗炎症治疗的高血压精准管理全景。

一、临床现状:全球高血压防控形势严峻,我国防治任重道远


根据世界卫生组织(WHO)2025年全球高血压报告,全球30~79岁成人高血压患者约14亿,是1990年的两倍多,每年导致约1100万人死亡,全球血压控制率不足四分之一[1]。全球血压控制率仅23%,仅加拿大、韩国、哥斯达黎加、冰岛控制率高于50%。全球血压控制率长期偏低的本质是“管理失败”(implementation failure),而不是单纯降压药物或治疗策略本身的问题。有学者因此提出了“Implementation Hypertension”概念,指那些按理说应该能被控制(有药物和监测手段、指南路径清晰)但实际仍未达标的高血压。WHO2025高血压报告和多个指南开始强调从“证据时代”(关注该用哪种药、控制到多少),走向“实施时代”(关注如何精准分型,如何在真实世界做好有效防控,精准治疗)[1]。
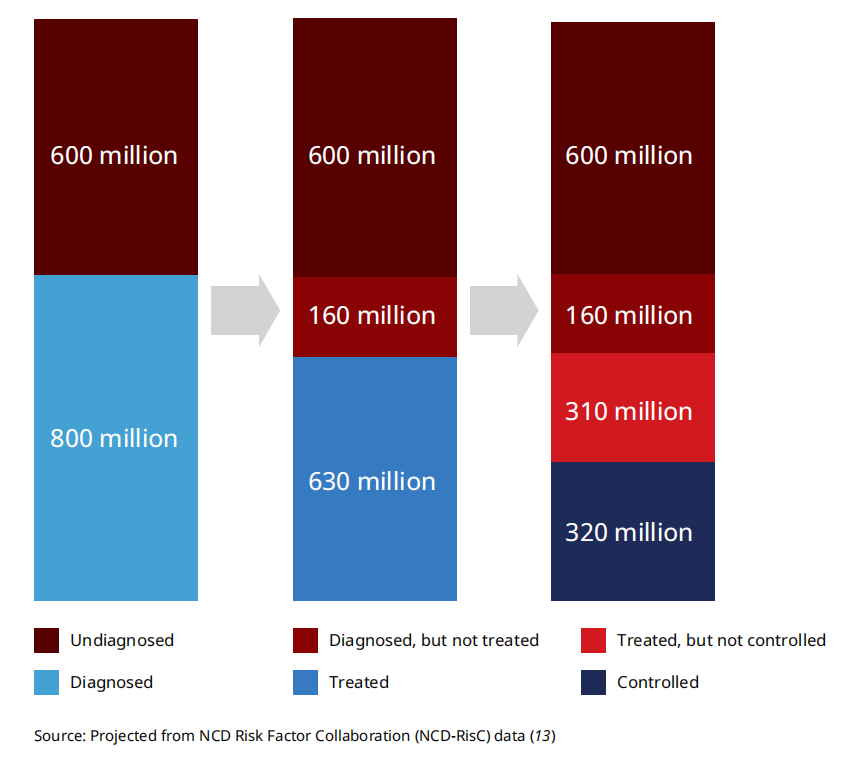
图1. 2024年全球30至79岁高血压患者数量,基于诊断、治疗和控制状态分类
我国数据显示,成人高血压粗患病率达31.6%,知晓率43.3%,治疗率38.7%,控制率仅12.9%,患者人数激增主要受人口增长、老龄化和患病率上升驱动,且男性远高于女性,中青年患病率上升明显。这一严峻现状的背后,是我们对高血压病理机制认知的局限。
事实上,近年来对高血压发病机制的深入研究,已揭示慢性低度炎症是其发生与进展的核心驱动因素,这一突破为治疗开辟了新思路。基于此,靶向抗炎治疗已不再停留于理论探索,而是继生活方式干预和传统药物治疗之后,高血压精准管理的全新策略与重要方向。这一理念也与新版《中国高血压防治指南(2024年修订版)》所倡导的精细化模式高度契合。指南明确提出,高血压管理已从单纯血压数值控制,升级为高血压的分级、分型、分类、分期及风险分层的精细化管理模式,强调降压、病因纠正、危险因素管控、靶器官保护、精准用药与个体化治疗的有机统一[2]。炎症免疫机制的深入探索,正是实现这一高血压精准防治和有效管理目标的关键突破口。
二、认知革新:慢性低度炎症是高血压发生发展的核心驱动因素


高血压状态下,机体免疫系统出现显著的失衡,主要表现为以下几个方面:
巨噬细胞极化异常:M1型促炎巨噬细胞过度活化,分泌TNF-α、IL-6等促炎因子,驱动血管炎症与重构;M2型抗炎巨噬细胞功能受损,炎症无法有效缓解。
T 细胞亚群失衡:Th17细胞过度激活、大量分泌IL-17,而Treg免疫抑制细胞功能下降,形成Th17/Treg失衡,进一步放大炎症反应。
中性粒细胞异常活化:通过释放炎症介质、产生氧化应激,直接参与血管损伤与靶器官损害。
炎症通路持续激活:NLRP3炎症小体、NF-κB等核心炎症通路异常活化,成为高血压炎症反应的“炎症开关”。
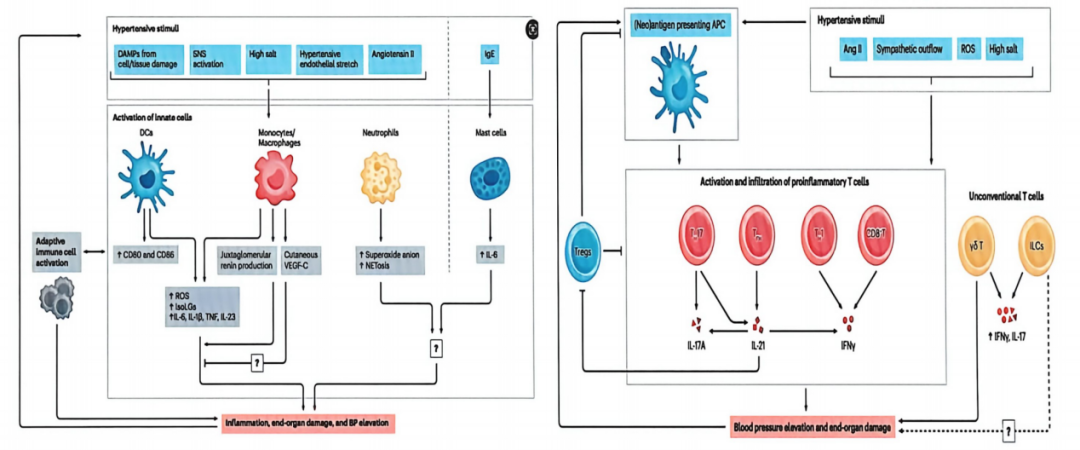
图2. 高血压免疫炎症级联反应机制
上述免疫炎症紊乱与交感神经系统(SNS)激活、肾素-血管紧张素-醛固酮系统(RAAS)亢进、氧化应激增强形成恶性循环,共同推动血压升高与血管病变进展[3],也为靶向抗炎降压提供了理论基础。
三、新近研究进展:克隆性造血、肠道菌群与铜死亡


01
克隆性造血:难治性高血压的炎症新视角
近期阜外医院汪一波教授团队在《Nature Aging》发表的研究发现,克隆性造血(CHIP)相关突变在难治性高血压患者中携带率高达23.23%。有趣的是,CHIP携带者血清中多种促炎细胞因子水平显著升高,包括IL-6、IL-16、MCP-1、TNF、IL-8和IL-1α等。中介分析提示,IL-1α和IL-16部分介导了CHIP对降压疗效的负面影响,提示炎症激活可能是CHIP促进抗高血压药物抵抗的关键环节[4]。这一发现为“炎症导致降压抵抗”提供了新证据,进一步阐明了难治性高血压发病的炎症免疫机制,也为未来开发针对克隆性造血相关炎症的靶向治疗、优化高血压患者个体化管理策略提供了重要依据。
02
肠道菌群调控:ARB治疗调节肠道菌群发挥靶器官保护作用
钟久昌教授团队在《iMeta》杂志发表的研究发现,血管紧张素受体阻滞剂(ARB)治疗可调节肠道微生物群,降低自发性高血压大鼠的收缩压水平。ARB重塑的肠道微生物移植(FMT)有助于调节高血压状态下的血清代谢组、肠道转录组及菌群代谢物,减少血管胶原沉积、炎症反应和氧化应激水平,减轻血管和肠道结构损伤[5]。这一发现揭示了肠道菌群紊乱与高血压血管重构损伤之间的密切关联,为高血压的综合管理提供了新思路。
03
铜死亡:高血压炎症损伤的新机制
钟久昌教授团队深入解析了铜死亡(Cuproptosis)这一新型细胞死亡方式在高血压损伤中的作用。研究证实,高血压及压力负荷状态下存在铜离子代谢异常,铜离子蓄积直接破坏线粒体功能并激活铜死亡通路,最终驱动血管重构与炎症损伤。
从机制干预来看,团队提出了多维靶向策略:一是铜离子螯合剂(如TTM)可直接清除过量铜离子、阻断铜毒性,有效改善高血压介导的铜死亡、心肌重构与心功能损伤[6];二是临床降压药物ACT-132577,可通过精准调控NEDD4-L-CTR1-铜信号通路,靶向抑制铜死亡通路激活,减轻炎症反应进而缓解压力负荷及高血压介导的血管重构损伤[7]。
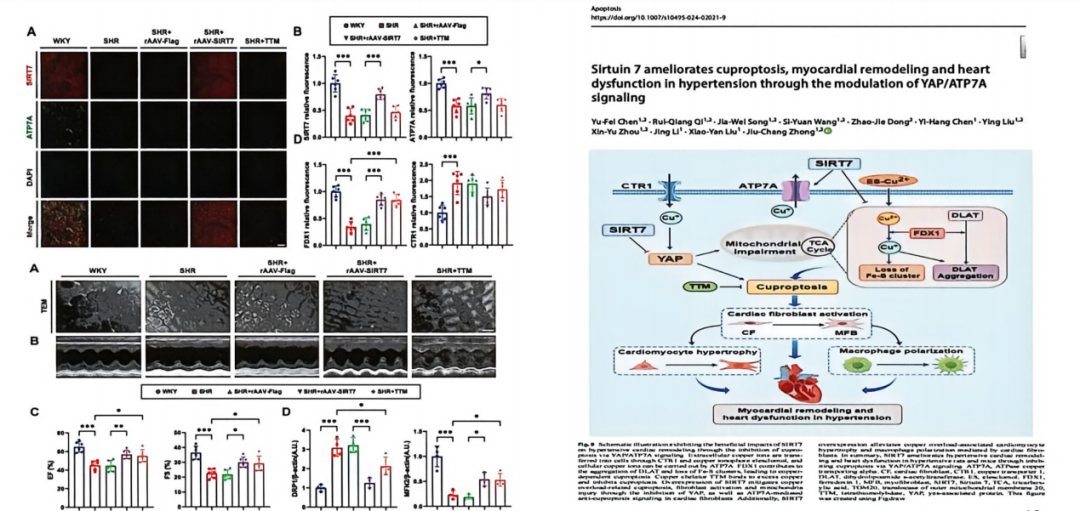
SIRT7通过YAP/ATP7A信号通路抑制铜死亡,改善高血压心肌重构与心功能障碍的机制
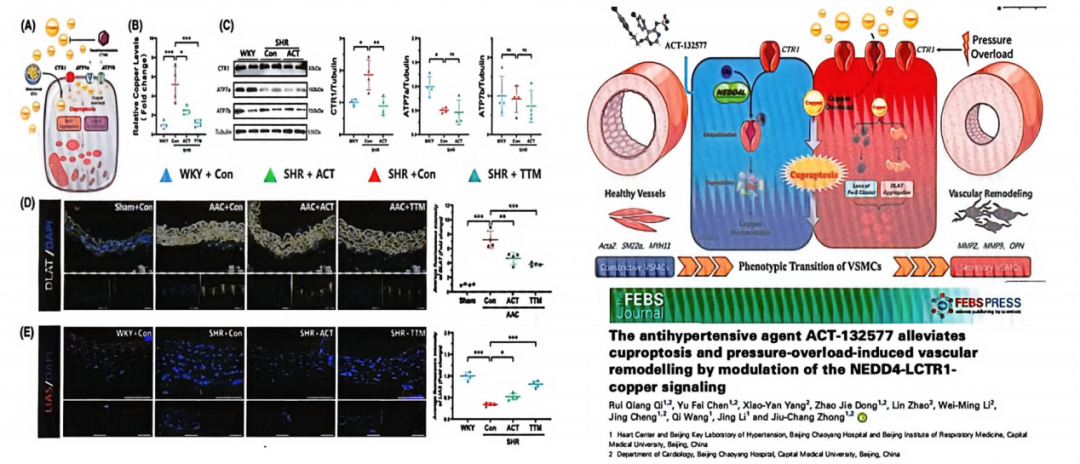
图3. ACT-132577通过调控NEDD4-L/CTR1-铜信号通路抑制铜死亡,改善压力负荷诱导的血管重构
这一系列发现揭示了铜代谢紊乱—铜死亡—靶器官损害的病理链条,为高血压精准治疗提供了新思路。
四、抗炎治疗:高血压靶向治疗的新希望


基于炎症在高血压中的核心作用,靶向抗炎治疗正在成为研究热点。
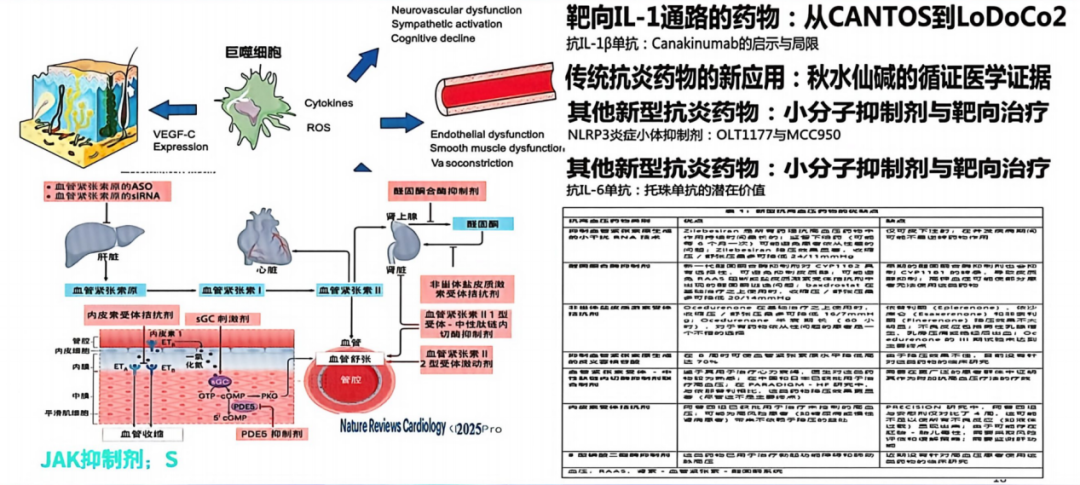 图4. 抗炎症治疗与高血压潜在药物靶点
图4. 抗炎症治疗与高血压潜在药物靶点
IL-1β通路:卡那单抗(Canakinumab)是IL-1β特异性单抗,在CANTOS研究中证实可降低心肌梗死后合并高敏C反应蛋白升高患者的主要心血管事件[8]。然而,其费用昂贵且严重感染风险增加,限制了临床普及。IL-1受体拮抗剂阿那白滞素(Anakinra)同样可有效降低ST段抬高型心肌梗死患者的炎症标志物水平,为抗炎干预提供了更多选择。
秋水仙碱:作为一种传统抗炎药物,LoDoCo2研究证实秋水仙碱可降低主要心血管事件31%[9]。其具有显著的成本优势,临床应用时需关注其可能出现的副作用。
其他潜在靶点:国内外大量研究表明,钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)被证实具备降糖、降压、减重功效的同时,还能发挥抗炎症作用;钟久昌教授团队研究证实,传统降压药物,如血管紧张素转换酶抑制剂(ACEI)、血管紧张素Ⅱ受体阻滞剂(ARB)以及针对内皮素系统新型降压药物双内皮素受体拮抗剂,均具有良好的抗炎症功效和心肾保护作用,其机制涉及抗铜死亡效应。铜与细胞之间的相互作用还可借助促炎信号通路(如NF-κB和STAT3)加重不良预后,可用于反映多种炎症相关疾病和心血管疾病发展过程并预测临床结局。
鉴于铜死亡在疾病中的双重作用,通过使用铜螯合剂或铜离子载体将细胞内铜浓度调节至毒性水平,有望成为新的治疗策略。联合应用细胞的存活与增殖能力,这有助于阐明铜死亡与心血管疾病进展之间复杂的多重关联。新型核酸药物如针对血管紧张素原(AGT)的siRNA干扰疗法,也在临床前和临床研究中均显示出良好的降压和抗炎效果。

小结


高血压防控正站在从经验管理走向机制干预、从单纯降压迈向精准治本的关键转折点。钟久昌教授的报告清晰地勾勒出一条从基础研究到临床转化的路径:揭示炎症免疫的核心驱动地位,拓展肠道菌群、铜死亡信号等新机制,验证靶向抗炎药物的可行性。另外,不同类型免疫细胞(Th1、Th2、T17细胞、TREG细胞、巨噬细胞、树突状细胞)可通过释放促炎细胞因子,影响血管的结构和功能,并直接或间接地影响肾脏的钠离子重吸收和体液平衡,从而调控机体血压水平。血管壁的炎症反应会导致血管内皮功能障碍和血管重构损伤,而肾脏的炎症则进一步影响其钠离子和水的排泄,这些都会导致高血压。因此,针对免疫-炎症-血管-肾脏轴的交互作用及其药物研发对高血压靶向抗炎治疗至关重要。
以CANTOS、COLCOT等临床试验为代表,针对炎症通路的药物干预,如卡纳单抗、秋水仙碱等,已展现出明确的心血管获益,开启了高血压抗炎治疗的新时代。未来,高血压的精准治疗将不再局限于“血压数值的达标”,而是通过精准分型深入到“病因的修正”与“靶器官的保护”。依托发病机制革新与治疗靶点突破,临床有望为不同亚型、不同分期、不同风险分层的高血压患者提供真正个体化的“治本”方案。这不仅是治疗手段的内涵提升,更是高血压防治理念的根本性变革,将为降低我国心血管疾病负担、推动心血管健康事业发展注入全新动力。
专家简介
钟久昌 教授
首都医科大学附属北京朝阳医院
现任北京市高血压重点实验室主任、北京市高血压创新工作室主任、首都医科大学附属北京朝阳医院心脏中心行政副主任、二级教授、博士生导师、博士后合作导师;2010-2017年度在上海交通大学医学院附属瑞金医院担任研究室主任,教授,博士生导师,曾兼任上海瑞金医院人力资源处副处长,2017年度按北京市人才引进加盟首都医科大学。先后担任中国生物医药产业链创新与转化联盟心脑血管药物工委会主任委员、中国中药协会微循环用药专委会副主任委员、中华医学会心血管病学分会高血压病学组与基础研究学组全国委员,中国药理学会表观遗传药理学专委会常务委员、中国老年学和老年医学学会老年病学分会常务委员、中国医促会外周血管病与难治性高血压分会常务委员、中国高血压联盟常务理事、中国老年医学学会高血压分会常务委员、北京慢病防治与健康教育研究会高血压分会副主任委员、北京中西医结合学会高血压防控专委会副主任委员及北京高血压防治协会秘书长。
主要从事高血压和心血管疾病药物靶点研究,先后承担国家科技重大专项课题、国家自然科学基金、北京市自然科学基金等20余项科研立项,其中主持国家自然科学基金项目10项。在Circulation、IMeta等上发表中英文论文100余篇,成果被国际著名期刊N Engl J Med等引用。授权国家发明专利5项。主编和参编《实用高血压学》等著作10余部。培养博士后、博士生及硕士生30余名。先后入选“全球前2%顶尖科学家“、首都医科大学科学技术奖、北京市高血压创新工作室领军人、北京市战略科技人才、北京市凤凰人才计划领军人才、上海市浦江人才、上海交通大学医学院双百人计划、上海交通大学优秀教师及首都医科大学优秀研究生导师奖。
参考文献:
2.中国高血压防治指南(2024年修订版)[J].?中华高血压杂志(中英文), 2024, 32(07): 603-700.
3.Gheblawi M, Wang K, Viveiros A, et al. Angiotensin-Converting Enzyme 2: SARS-CoV-2 Receptor and Regulator of the Renin-Angiotensin System: Celebrating the 20th Anniversary of the Discovery of ACE2. Circ Res. 2020 May 8;126(10):1456-1474.
4.Lv C, Wang H, Yu L, et al. Clonal hematopoiesis in apparent treatment-resistant hypertension, insights from multiple medical centers and community-based cohorts. Nat Aging. 2025 Dec;5(12):2466-2481.
5.Li J, Wang SY, Yan KX, et al. Intestinal microbiota by angiotensin receptor blocker therapy exerts protective effects against hypertensive damages. Imeta. 2024 Jul 18;3(4):e222.
6.Chen YF, Qi RQ, Song JW, et al. Sirtuin 7 ameliorates cuproptosis, myocardial remodeling and heart dysfunction in hypertension through the modulation of YAP/ATP7A signaling. Apoptosis. 2024 Dec;29(11-12):2161-2182.
7.Qi RQ, Chen YF, Yang XY, et al. The antihypertensive agent ACT-132577 alleviates cuproptosis and pressure-overload-induced vascular remodelling by modulation of the NEDD4-LCTR1-copper signaling. FEBS J. 2026 Apr;293(7):1930-1950.
8.Ridker PM, Everett BM, Thuren T, et al. Antiinflammatory Therapy with Canakinumab for Atherosclerotic Disease. N Engl J Med. 2017 Sep 21;377(12):1119-1131.
9.Nidorf SM, Eikelboom JW, Budgeon CA, et al. Low-dose colchicine for secondary prevention of cardiovascular disease. J Am Coll Cardiol. 2013 Jan 29;61(4):404-410.



我要留言