编者按:高血压与慢性肾脏病(CKD)常如影随形,互为因果,导致临床治疗陷入“难治性”困境,显著增加患者心血管事件及终末期肾病(ESRD)风险。肾去神经术(RDN)作为近年来备受关注的微创介入技术,为打破这一恶性循环提供了全新视角。中华医学会第二十四次介入心脏病学大会(CIT 2026)上,首都医科大学附属北京安贞医院王运红教授报告了高血压合并CKD患者中的特征、临床管理现状及RDN的应用价值,为临床实践提供前沿思考。

一、互为因果的困境:高血压与CKD的恶性循环
01
病理生理机制双向驱动
高血压与慢性肾脏病之间存在密切的双向关系,两者相互促进,形成难以打破的恶性循环。从病理生理机制来看,长期的高血压会导致肾小动脉硬化,进而引起肾缺血和肾单位毁损;而肾脏受损后,水钠潴留和肾素-血管紧张素-醛固酮系统(RAAS)的过度激活又会反过来推高血压。
02
高患病率加剧临床负担
回顾1999年至2018年的美国数据,高血压患者中各期CKD的患病率始终居高不下(图1),且白蛋白尿和大量白蛋白尿的患病率维持在较高水平[1]。这表明在高血压群体中,肾脏损害是一个极为普遍的现象。这种高患病率不仅意味着医疗资源的巨大消耗,更预示着未来心血管事件的高发风险。
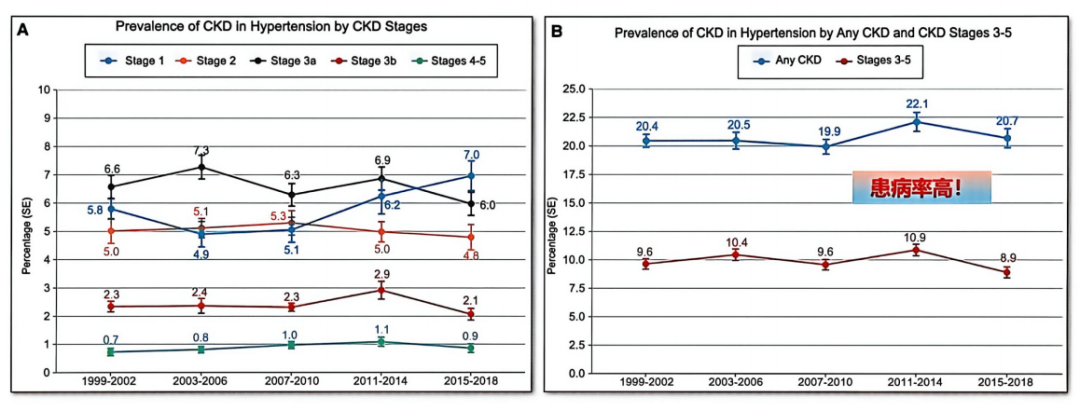
图1. 1999年至2018年美国成年高血压患者中CKD各期的患病情况
03
隐蔽性特征增加诊疗难度
隐蔽性高血压/隐蔽性未控制高血压在CKD患者中非常常见。数据显示,约56%服用降压药物的CKD患者存在隐蔽性未控制高血压[2],这意味着靶器官损害可能在不知不觉中悄然进展。CKD患者的血压节律紊乱更为常见且严重:非勺型血压、夜间高血压及清晨高血压显著增多,且随着肾功能的恶化,这种节律异常呈现加剧趋势。而夜间高血压是心血管死亡的独立预测因子,其高发进一步加剧了患者的预后风险。此外,无论是否接受透析,CKD患者的血压均存在明显的季节性变异,这种随季节波动的特性增加了长期血压管理的复杂性。
难治性高血压(RH)与ESRD风险的激增是这一恶性循环的最终结局,也是临床最为棘手的问题。多重机制如糖尿病、老年、肥胖、药物源性因素等共同导致了CKD患者中难治性高血压的高发(图2)。在中国,维持性血液透析患者中约三分之一合并难治性高血压。面对这一困境,单纯增加药物剂量往往效果不佳且副作用显著增加,临床亟需新的治疗策略来打破这一僵局。
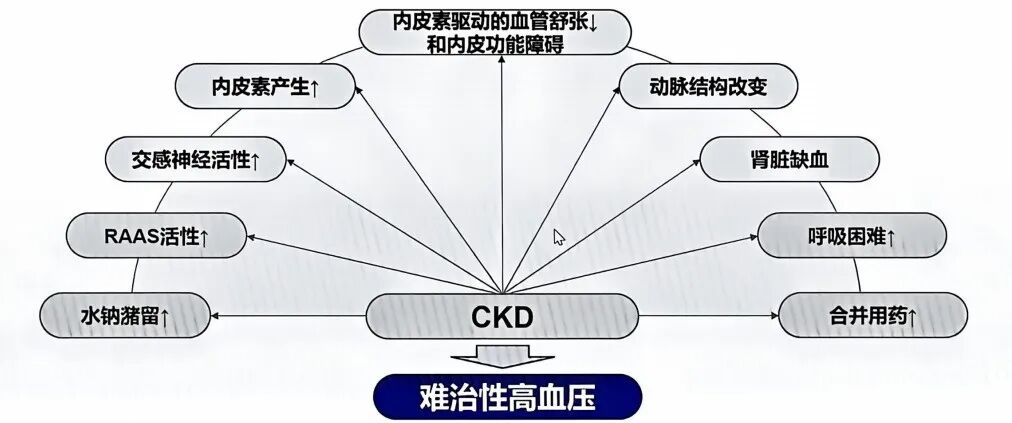
图2. 多重机制共同导致CKD患者RH高发
二、未被满足的需求:CKD合并高血压的管理现状
01
个体化降压目标
纵观不同指南,虽然对于血压控制目标的具体数值存在差异(图3),但总体趋向于个体化强化控制。《2024中国高血压临床实践指南》根据蛋白尿水平进行了精细分层,对于蛋白尿>300 mg/24h的患者推荐<130/80 mmHg的目标,如能耐受SBP可降至120mmHg,而对于蛋白尿较低者则推荐<140/90 mmHg,如能耐受SBP可降至130mmHg,并强调了早期干预的重要性[2]。
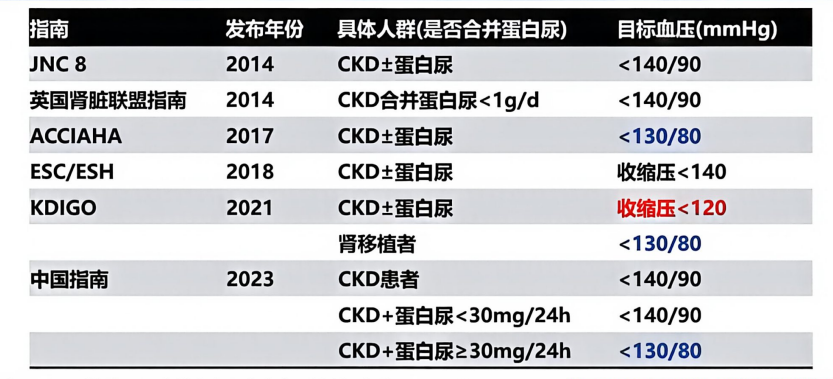
图3. 不同指南的降压目标
2
强化降压的获益与风险
针对SPRINT及ACCORD-BP研究的事后分析表明,强化血压控制(收缩压<120 mmHg)可显著降低基线存在CKD患者的肾衰竭风险54%(HR:0.46),增加估算肾小球滤过率(eGFR)下降≥30%的风险,但降低了白蛋白尿的发生风险[4]。因而,强化血压控制可能增加轻度CKD进展的风险,但不会增加更严重阶段CKD进展或肾衰竭的风险。
03
药物治疗原则
高血压的药物治疗应遵循以下整体原则(图4):以标准剂量起始(老年人可酌情减量)、根据血压分级与心血管风险分层确定起始治疗方案、优先选用长效降压药并制定个体化治疗策略。药物选择方面,单药治疗初始首选ACEI/ARB类药物(不建议两者联用),亦可选用CCB、β受体阻滞剂或α1受体阻滞剂;其中α/β受体阻滞剂兼具心肾双重保护优势,各类药物可根据临床实际情况酌情联合使用。

图4. 高血压的治疗策略
CKD合并RH时,需先评估CKD分期及尿蛋白水平:对于CKD 1~3期患者,治疗以ACEI/ARB/ARNI为基础,初始推荐ACEI或ARB联合CCB(A+C方案)或利尿剂(A+D方案);若血压未达标,则采用A、C、D三药联合方案;仍未达标时,可加用螺内酯、α/β受体阻滞剂等药物,必要时还可选用新型MRA、SGLT-2i或GLP1-RA;CKD 4~5期患者需谨慎使用ACEI/ARB/ARNI并加强监测,优先选用袢利尿剂,并结合肌酐、eGFR水平调整用药方案;部分患者若无透析保障,推荐以CCB为基础联合α/β受体阻滞剂。整体治疗策略中,两药联合(A+C或A+D方案)为初始推荐方案,三药联合(ACEI/ARB+CCB+利尿剂)适用于两药控制效果不佳的患者,四药及以上联合时可加用螺内酯等药物,应注意避免高钾血症。然而,即便采用多药联合方案,RH患者的血压控制仍往往难以达标,且会增加副作用发生风险。因此,临床上迫切需要新的治疗手段来补充甚至替代传统药物治疗。
三、破局重生的希望:
RDN循证医学证据与临床实践探索
01
RDN围手术期管理策略
肾去神经术(RDN)作为一种微创介入技术,是改善难治性或未控制高血压的有效选择。在围手术期管理方面,术前需全面评估肾动脉解剖,确保手术可行性;术中需充分水化以预防造影剂肾病,保护残余肾功能;术后需继续药物治疗并至少加用抗血小板治疗一个月,以预防血栓形成。对于透析患者,需精心安排透析时机并密切监测血压波动;对于肾移植患者,现有小样本研究证据探索了谨慎适度的RDN治疗可能具有获益,为特殊人群的管理提供了指导[5]。
02
RDN疗效在部分CKD患者中显现
Global SYMPLICITY注册登记研究纳入2237例RDN患者,其中1742例完成3年随访。基于eGFR分层分析显示,RDN长期疗效显著:各亚组降压效应持续3年,nCKD和CKD3a组血压持续下降,CKD3b组舒张压明显降低。CKD3b组降压药物使用减少,实现药物减负。肾功能方面,CKD3a和3b组eGFR下降幅度相近,肾功能稳定,验证了RDN安全性。但CKD4期患者降压获益在不同个体中差异较大,部分患者因肾动脉萎缩或灌注不足,消融操作困难,术前影像学精准评估显得尤为重要[6,7]。
我国单中心数据进一步验证了NetrodRDN系统的疗效,纳入CKD患者(1~5期),术后6个月随访时,诊室血压及24小时动态血压均显著下降,6个月时平均24h血压下降幅度达18.0/9.3 mmHg。在安全性方面,术后肾功能无显著变化,多普勒扫描显示无肾动脉狭窄或血流受限,且无器械相关并发症发生[8]。
03
特殊人群的RDN应用拓展
对于非透析患者,RDN不仅能有效降低血压,还可降低肾阻力指数,并减少微量及大量白蛋白尿患者的比例,提示其或许具有超越降压效果之外的肾脏保护作用。对于透析患者而言,目前尽管证据较少,但小样本探索性研究显示,RDN似乎是治疗透析患者严重高血压的一种有效且安全的选择,既不影响透析耐受性,也不会干扰贫血、CKD-MBD的治疗,还有助于减轻患者的药物负担,为后续肾移植创造有利条件。对于肾移植患者,RDN治疗组的诊室收缩压显著下降,夜间血压降低效果同样明显,且非杓型血压转变为杓型血压的患者比例显著提升,这对改善移植肾的长期预后具有关键意义。
目前,由北京安贞医院牵头的一项全国多中心临床研究(拟入组236例)正有序推进,旨在验证RDN应用于“未被控制的高血压合并慢性肾脏病”患者的有效性与安全性,为全国乃至全世界提供中国证据。
结语
高血压与CKD的恶性循环是临床治疗的难点,而肾去神经术(RDN)的出现为打破这一困局带来了曙光。从国际注册研究到中国单中心数据,RDN在不同分期的CKD患者中均表现出良好的降压效果、肾脏安全性及药物减负潜力。RDN有望成为高血压合并CKD患者综合管理中的重要武器,为改善患者预后带来新的希望。


(来源:《心肾代谢时讯》编辑部)


我要留言