编者按: “心血管-肾脏-代谢综合征”(CKM)概念的提出,揭开了一个长期被忽视的临床真相:心血管疾病、慢性肾脏病和代谢异常——这三个看似独立的系统,实则共享同一条代谢炎症通路。为描述这一多系统损害的累积效应,该框架采用0~4期的分期系统,试图将碎片化的风险整合为连续的疾病演进图谱。但问题随之而来:这个分期框架可以预测死亡风险吗?每一期的风险到底高出多少?不同人群的答案是否一样?
近日,发表于American Journal of Preventive Cardiology的一项系统综述与Meta分析,首次基于超千万人群的研究数据,明确证实CKM分期与全因死亡、心血管死亡等结局存在清晰的剂量-反应关系,同时揭示性别、年龄、教育水平对该关联的显著影响,为CKM分期从“概念框架”向临床可操作的风险分层工具转化,提供了迄今为止最全面的循证依据。

概念之争:从“代谢综合征”到“心血管-肾脏-代谢综合征”
代谢综合征的概念我们耳熟能详——高血压、高血糖、血脂异常、中心性肥胖,满足三项即可诊断。但问题是,这个框架忽略了两个关键系统:心血管和肾脏。
真实的临床图景远比这复杂。临床实践中,肥胖合并2型糖尿病的患者,往往同时伴有高血压和早期肾功能损伤。这三个系统相互影响——肾脏损伤加重高血压,高血压加速血管硬化,血管硬化进一步损害肾脏和心脏。这是一个闭环,不是三条平行线。
为了更好地描绘这种复杂的临床状态,美国心脏协会于2023年正式提出心血管-肾脏-代谢综合征(CKM综合征)的新概念,其核心定义是:至少存在心血管疾病、慢性肾脏病、2型糖尿病或肥胖中的两种。这一定义超越了传统的“合并症”思维,强调三者之间的双向互动与协同恶化。
为描述这一多系统损害的累积效应,CKM框架采用0至4期的分期系统:
0期:无任何危险因素的健康状态;
1期:存在超重/肥胖、代谢异常等早期风险因素;
2期:出现中度至高风险的代谢风险、严重的胰岛素抵抗或早期肾功能损伤;
3期:存在亚临床心血管疾病或极高危慢性肾脏病;
4期:已合并临床心血管疾病和肾功能衰竭的终末阶段。
CKM综合征的提出,正是要打破“各管一段”的思维定式,将碎片化的风险整合为连续的疾病演进图谱。但这一框架对患者预后评估的价值,一直缺乏大规模数据的量化验证。
Meta分析核心发现:
死亡风险随分期进展呈“阶梯式”攀升
为了量化CKM分期进展与死亡风险之间的关联,研究者开展了一项大规模系统综述与Meta分析。研究者系统检索了PubMed、Embase、Web of Science和Cochrane图书馆四大数据库,纳入2023年1月~2025年8月发表的前瞻性或回顾性队列研究,最终筛选出9项符合标准的研究,总样本量高达10 330 498例,覆盖中国、美国、英国等多个国家的代表性人群,旨在评估随着CKM分期,全因死亡、心血管死亡、冠心病死亡和卒中死亡的风险究竟升高多少。
研究发现,死亡风险随CKM分期进展呈“阶梯式”攀升。
1
全因死亡:4期风险激增2.8倍
与0期相比(图1):
2期:风险增加40%(HR=1.40);
3期:风险增加191%(HR=2.91);
4期:风险增加282%(HR=3.82)。
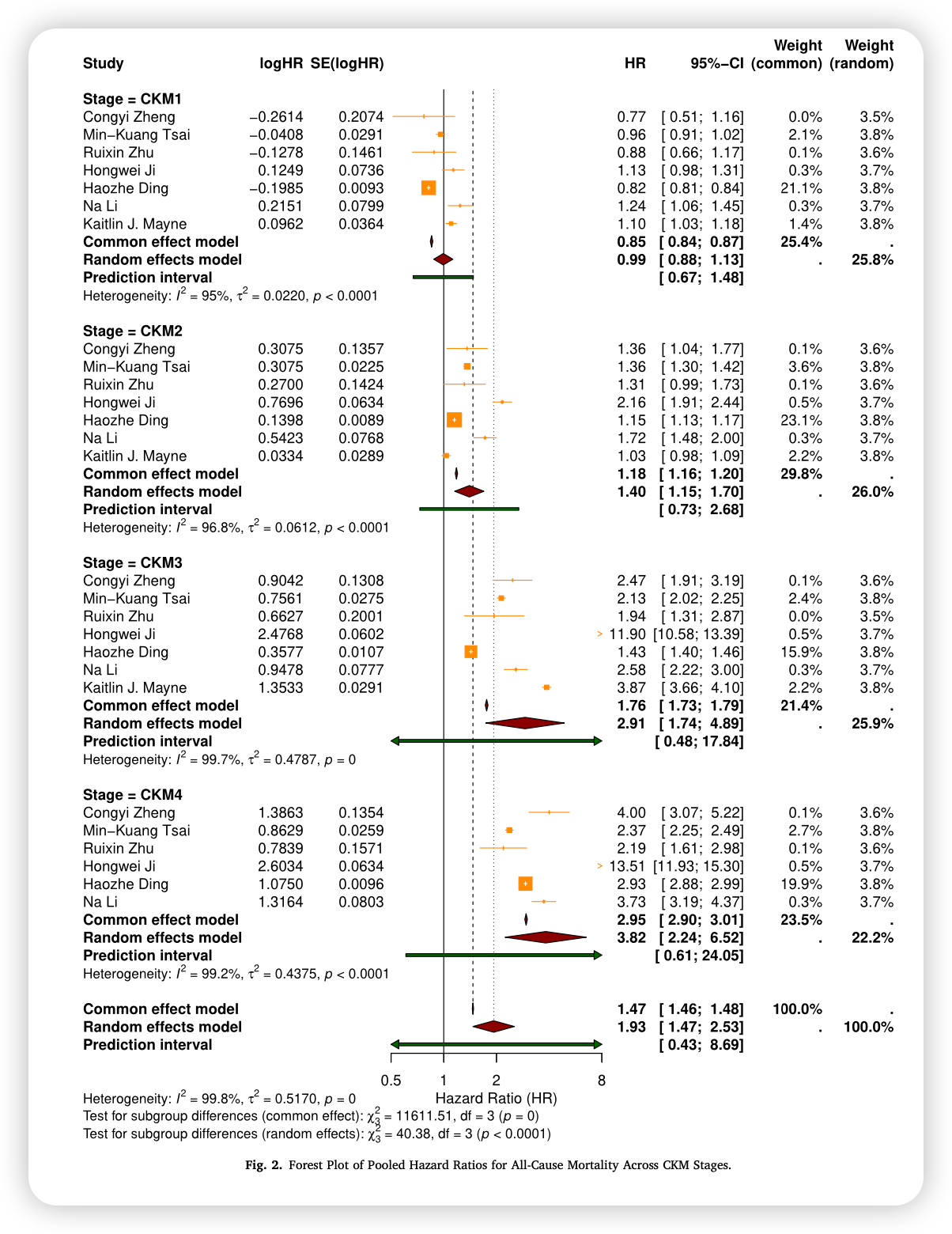
图1. 全因死亡率在不同CKM分期的合并风险比
这意味着,当一个患者从无任何危险因素(0期)进展到已有临床心血管病合并肾功能衰竭(4期)时,全因死亡风险升高近3倍。
2
心血管死亡:4期风险激增5.4倍
心血管死亡的增幅更为陡峭:
1期:风险增加15%(HR=1.15);
2期:风险增加113%(HR=2.13);
3期:风险增加305%(HR=4.05);
4期:风险增加538%(HR=6.38)。
从2期到3期,从3期到4期,心血管死亡风险持续增长——这是真正的“雪崩效应”。
3
冠心病死亡与卒中死亡:晚期急剧升高
冠心病死亡:4期风险是0期的9.2倍(HR=9.19);
卒中死亡:4期风险是0期的5.5倍(HR=5.48)。
值得注意的是,冠心病死亡在4期的风险增幅远超其他结局,提示心血管系统在CKM晚期成为最脆弱的靶器官。
真实世界的多样性:性别、年龄、教育水平如何改写死亡风险
研究还发现,CKM分期与死亡风险的关联并非“一刀切”,而是被三个关键因素深刻修饰:
1
性别:女性全因死亡更高,男性心血管死亡更陡
全因死亡:女性在各分期的风险均略高于男性;
心血管死亡:呈现分期特异性差异——女性在2期风险更高,男性在3期风险更高,至4期两者持平。
研究者分析,女性绝经后雌激素水平下降可能加速代谢、肾脏和血管功能障碍;而男性在中晚期心血管死亡风险陡升,可能与高血压、吸烟、饮酒和内脏脂肪堆积的更高负荷有关。
2
年龄:每增加1岁,心血管死亡风险增加3.8%
年龄是心血管死亡的显著效应修饰因子。Meta回归分析显示,平均年龄每增加1岁,心血管死亡风险增加约3.8%。年龄因素解释了约22.47%的研究间异质性,表明其对CKM相关死亡风险的显著影响。
进一步的分层分析显示,高龄组(≥62.5岁)的合并风险(HR=3.29)显著高于低龄组(HR=1.79)。这意味着,同属CKM 4 期的患者,高龄人群面临更高的心血管死亡风险,衰老带来的代谢失调、肾功能自然下降与血管重塑,进一步放大了CKM的病理损害。
3
教育水平:低教育程度放大所有死亡风险
研究还发现,社会环境因素尤其是受教育程度,在 CKM 综合征分级与死亡风险的关联中发挥了深刻的调节作用 。
元回归分析显示低教育程度显著放大了 CKM 综合征的致死风险(图2) :
全因死亡:低教育组HR=1.98 vs. 高教育组HR=1.54;
心血管死亡:低教育组HR=3.69 vs. 高教育组HR=2.47;
冠心病死亡:低教育组HR=1.45 vs. 高教育组HR=1.12;
卒中死亡:低教育组HR=1.38 vs. 高教育组HR=1.10。
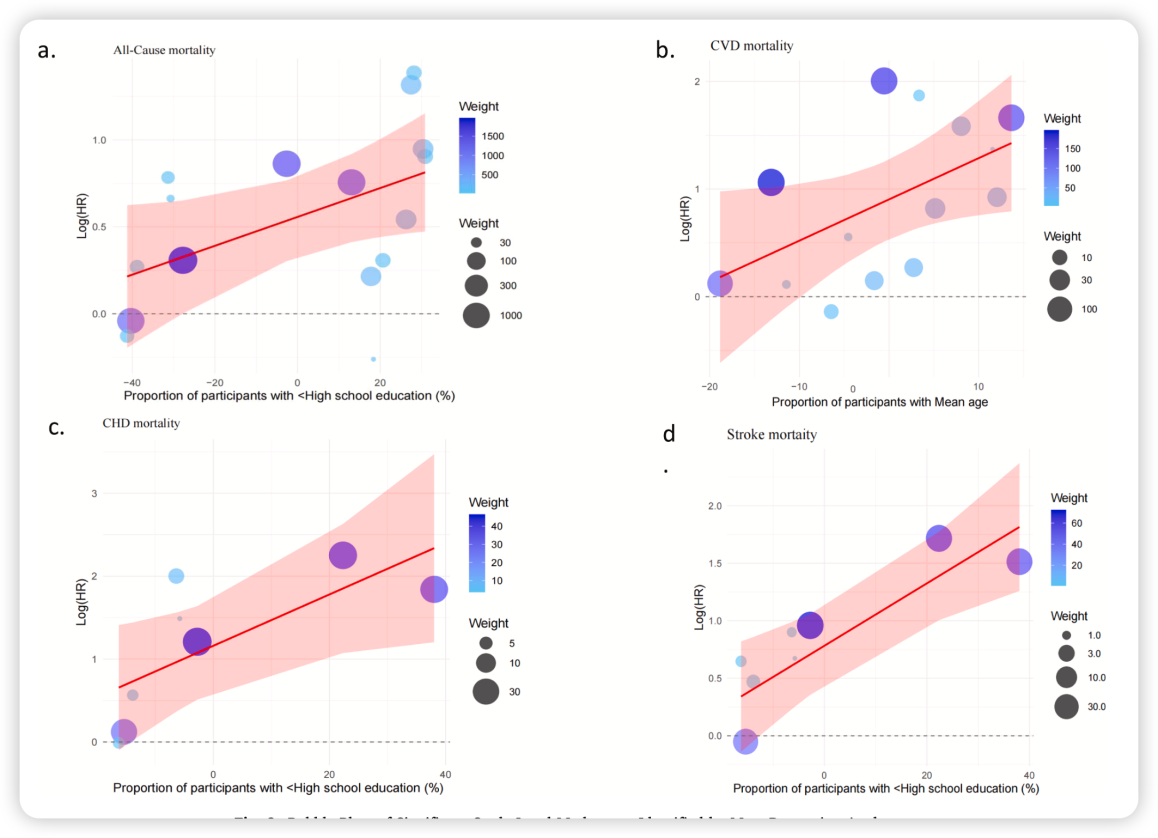
图2. 通过元回归分析确定的显著研究层面调节变量的气泡图
教育程度的差异显著解释了研究间观察到的异质性:分别贡献了全因死亡异质性的 25%、冠心病死亡的 55% 以及卒中死亡的 68% 。
临床意义:从概念框架到风险分层工具
本研究的核心价值在于首次为CKM分期的预后价值提供了大规模定量证据,为临床实践带来多重启示:
1
早期识别窗口:2期是关键转折点
研究发现,从2期开始,各项死亡风险出现显著升高。这意味着,当患者刚刚出现代谢异常合并早期肾功能损伤时,正是启动综合干预的最佳窗口期。抓住这一时机,或可阻断多系统损害的进一步累积。
2
性别特异性风险管理
性别分层分析揭示了截然不同的风险轨迹:
女性患者:在各CKM分期的全因死亡风险均略高于男性,需关注代谢和肾功能障碍早期的系统性风险升高,在CKM早期阶段即加强综合管理。
男性患者:在CKM中晚期心血管死亡风险上升更陡峭,需重点防控中晚期心血管事件,尤其是在3期向4期进展的关键阶段。
3
将衰老机制纳入未来风险评估框架
这一模式反映了年龄相关的代谢失调、肾功能下降和血管重塑的累积效应。将衰老机制纳入未来风险评估框架,对于提升CKM管理的精准性至关重要。
4
社会决定因素不容忽视
教育水平对死亡风险的放大效应提示我们,CKM管理不应仅限于药物。改善健康素养、提高医疗可及性、减少慢性应激暴露——这些“非医学干预”同样是降低CKM相关死亡的重要组成部分。
结语:CKM分期——不止是概念,更是行动指南
这项覆盖超千万人群的Meta分析证实,CKM分期与各类死亡风险存在明确的剂量-反应关系,且风险随分期呈阶梯式攀升,其中性别、年龄和教育水平等因素显著修饰这一关联,揭示了CKM综合征是生物、行为与社会因素共同作用的结果。对临床医生而言,CKM分期提供了实用的动态风险监测工具,其核心价值在于推动疾病管理关口前移,实现早期风险识别、精准干预与进展阻断。
参考文献:Ding H, Jiang L, Zhao Y, Lee D, Chun B. Associations between cardiovascular-kidney-metabolic syndrome staging and risks of all-cause and cardiovascular mortality: a systematic review and meta-analysis. Am J Prev Cardiol. 2026;25:101407.
点击左下角“阅读原文”可查看文章原文


(来源:《心肾代谢时讯》编辑部)

我要留言