编者按:
原发性醛固酮增多症(PA)一直被视为心肾损害的“超级风口”,其临床治疗面临着难以逾越的鸿沟。随着介入治疗技术的飞速发展,这一僵局正在被打破。中华医学会第二十四次介入心脏病学大会上,南昌大学第二附属医院董一飞教授带来了题为《肾上腺消融治疗高血压的技术可行性》的前沿分享。他指出,经皮超选择性肾上腺动脉消融/栓塞术(SAAE),这一历经近30年探索的技术,正从“姑息治疗”走向“精准治愈”,有望填补特发性高醛固酮血症(IHA)与醛固酮腺瘤(APA)治疗的巨大空白。

一、历史回眸:30年探索奠定“介入治疗”的可行性
SAAE是近年来迅速发展起来的治疗PA的血管内介入技术。其原理是通过微导管超选择性插入肾上腺病变组织的供血动脉,注入栓塞剂或消融剂,使病变组织缺血坏死,从而减少醛固酮的过度分泌。该技术对IHA和APA患者均具有一定的治疗潜力。
这项技术并非横空出世的“新概念”,而是一场跨越近30年的医学马拉松。从早期的个案报道,到队列研究,再到如今的随机对照试验,SAAE的证据链条正在日益完善。董一飞教授指出,回顾这30年的文献,SAAE几乎覆盖了PA的所有亚型——无论是单侧的APA,还是双侧的IHA,甚至是混合型病例,都有了相应的介入治疗探索。
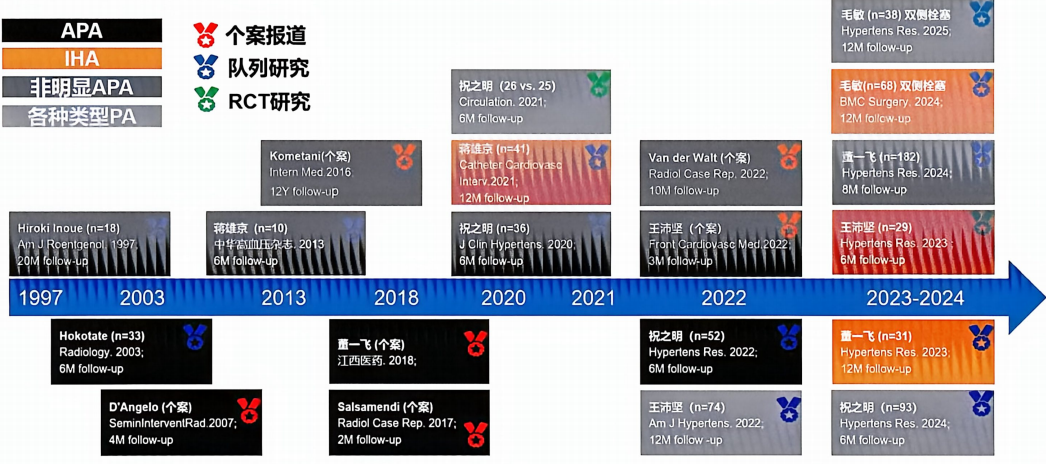
 图1. SAAE的全证据链
图1. SAAE的全证据链
这种长期的临床积累,为SAAE在有效性与安全性上的可行性奠定了坚实的基础。它不再仅仅是外科手术的替代方案,更是一种独立的、针对特定人群的精准治疗手段。
二、临床疗效:SAAE能带来多大获益?
SAAE的临床疗效已经得到多项研究一致证实。汇总全球650例患者的分析结果显示,SAAE治疗后患者收缩压平均下降19.84 mmHg,舒张压平均下降10.62 mmHg,血浆醛固酮平均下降90.99 pg/mL,血钾平均升高0.59 mmol/L,中位随访时间约6个月,整体疗效稳定可靠[1]。
尽管SAAE的有效性判断标准在不同研究中各异,目前少量研究采用国际PASO标准进行SAAE术后疗效评估:APA患者接受SAAE治疗后的完全临床成功率可达17.6%~54.2%,生化完全成功率可达44.4%~80%;即便是既往认为手术不获益的IHA患者,SAAE也可达到12.9%~28.6%的完全临床成功率和33.8%~67.6%的生化完全成功率,显著突破了传统治疗的适用边界。
三、机制深潜:超越血压的“心肾获益”密码
SAAE的价值不仅在于血压计上的数字,更在于它对靶器官的深层保护。董一飞教授通过团队的多项研究,揭示了SAAE在逆转心肌重构和改善肾功能方面的独特机制。
1
对左心室重构的影响
研究团队纳入了一组IHA患者(传统认为手术无效),随访12个月后发现:在两组患者术后24小时动态血压完全一致的情况下,生化完全缓解组(醛固酮恢复正常)的左心室质量指数和左心室舒张末径均显著下降,而生化部分/未缓解组则无此变化[2]。
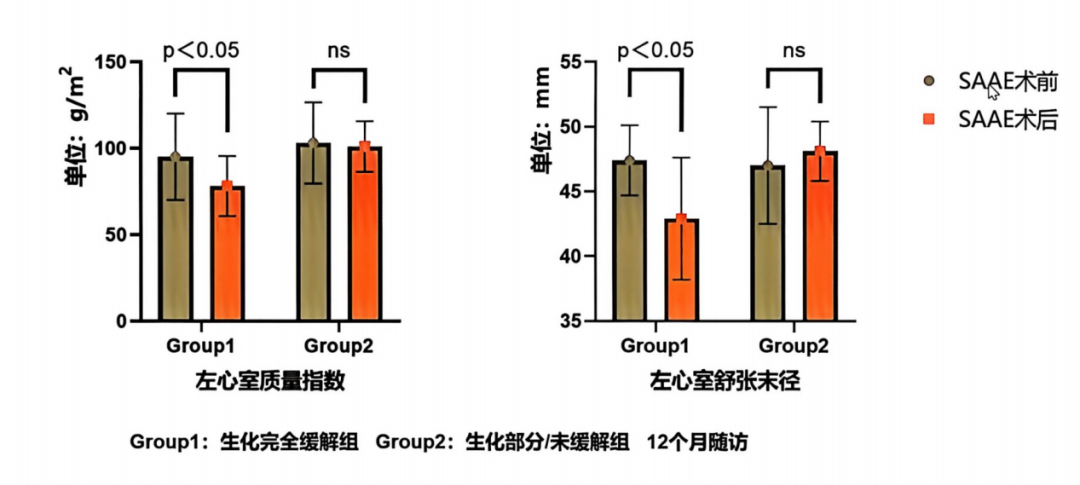
图2. SAAE治疗12个月随访:不同生化缓解状态患者左室结构指标变化对比
进一步延长随访至25个月,生化完全缓解组的左心室质量指数下降更为显著[3]。
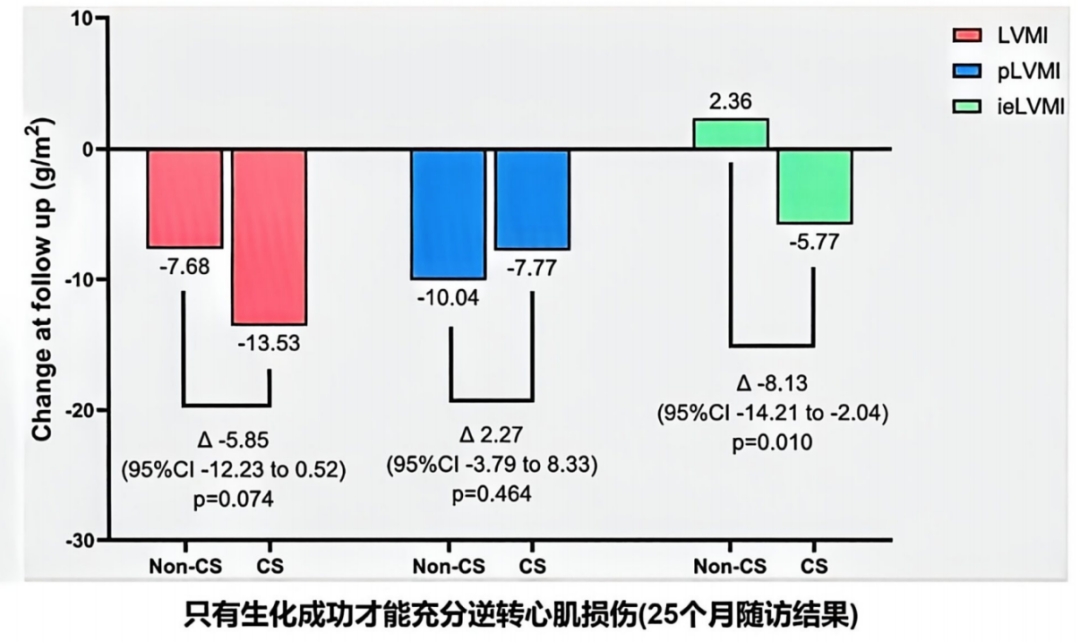
图3. SAAE治疗25个月随访:生化成功(CS)与未生化成功(Non-CS)患者左室肥厚指标变化对比
通过统计模型分析,研究进一步发现左室重构的改善,不仅取决于血压下降的血流动力学效应,同时取决于醛固酮水平的恢复。这意味着,SAAE通过对肾上腺病灶的功能学改良,从根源上逆转了心脏的病理改变。
2
对肾功能的影响
团队分析了182例接受SAAE治疗的患者,根据术前eGFR进行分组。总体来看,术后eGFR有轻度下降,但分层分析揭示了一个重要现象:eGFR的下降主要来源于术前存在肾小球超滤过(即eGFR高于预期正常值上限)的患者[4]。
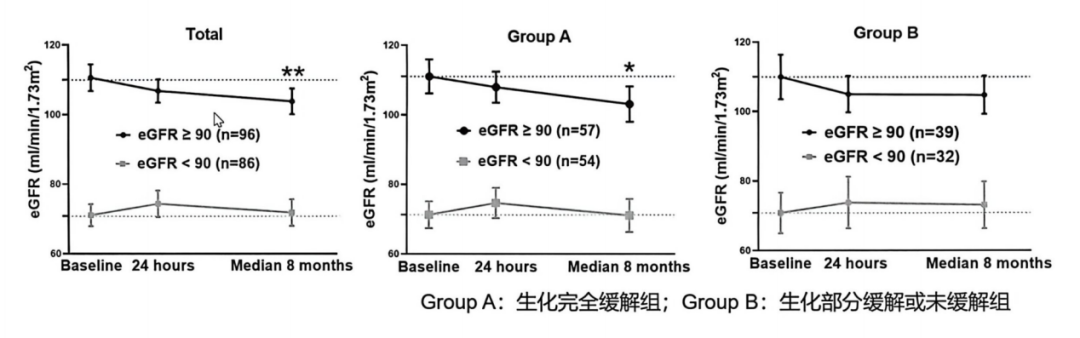
图4. SAAE治疗前后eGFR变化:基线肾功能与生化缓解状态对长期肾功能的影响
超滤过是PA早期肾损害的核心标志,常伴随微量白蛋白尿。SAAE术后eGFR的轻度下降,并非肾功能的实质性损伤,而是对原醛症特征性肾脏高滤过状态的有效纠正。随着术后醛固酮水平恢复正常,肾脏的高灌注、高滤过状态随之消退,eGFR逐步回落至生理范围,从根本上避免了长期高滤过介导的肾小球硬化进展,是对肾功能的长期保护。
3
对血压节律的影响
研究团队发现,接受SAAE治疗后,患者全天血压水平均显著下降,且夜间血压的下降幅度大于白天。这一现象对高血压高质量管理具有重要意义——夜间血压是心血管风险的独立预测因子[2]。
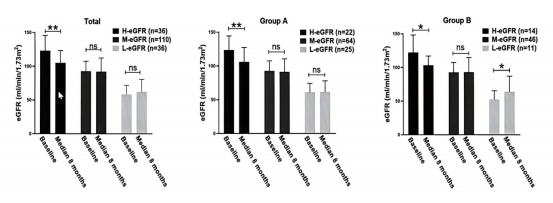
图5. PA患者接受SAAE后中位随访8个月,不同基线eGFR亚组的肾功能变化,其中H-eGFR组变化最为显著(P<0.001)
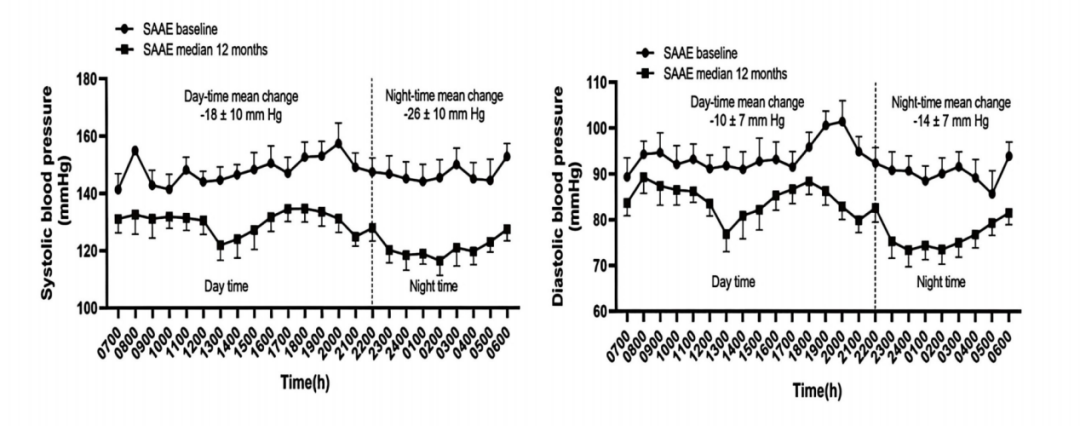 图6. SAAE的应用对血压节律的影响
图6. SAAE的应用对血压节律的影响
进一步分析680余例患者的数据发现:醛固酮水平越高,夜间血压下降幅度越小,越容易呈现“非杓型”甚至“反杓型”血压节律。随后,团队将部分患者按SAAE术后醛固酮是否完全恢复正常进行分组,结果发现:只有醛固酮完全恢复正常者,其夜间血压节律才会出现统计学上显著的改善[5]。这再次印证了“醛固酮完全正常化”对于靶器官保护的核心价值。
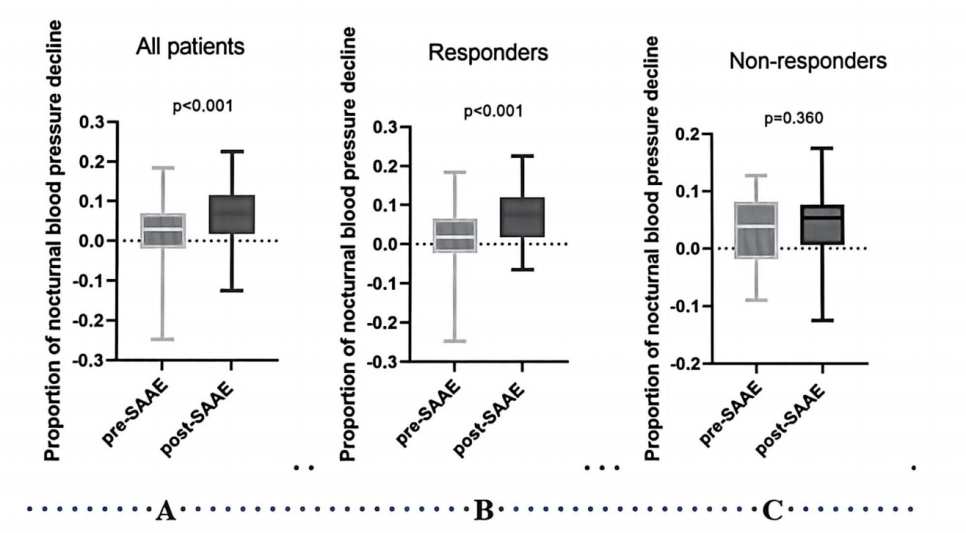 图7. SAAE治疗前后夜间血压下降比例变化,仅生化应答者组实现血压节律显著改善
图7. SAAE治疗前后夜间血压下降比例变化,仅生化应答者组实现血压节律显著改善
4
对肾上腺功能的影响
临床数据显示,SAAE在显著降低醛固酮水平的同时,对皮质醇、性激素及儿茶酚胺等其他肾上腺激素水平并无明显影响[6-8]。这意味着该技术实现了对病变组织的“定点清除”,完整保留了肾上腺的正常内分泌功能。结合近30年的文献回顾,SAAE的严重不良事件发生率极低,这种“去功能而不伤器官”的特性,使其成为了一种兼顾疗效与安全的理想治疗选择。
四、临床定位:SAAE有望成为PA第三种标准治疗方案

基于充分的循证证据与临床实践,SAAE不应再被视为探索性技术,而具备成为PA第三种标准治疗方案的潜力,与药物治疗、外科手术并列。其最适合的人群包括:药物治疗效果不佳或无法耐受盐皮质激素受体拮抗剂的患者;无法耐受外科手术或拒绝手术、希望微创治疗的患者;影像学有定位表现但肾上腺静脉采血(AVS)阴性或无明确侧化的患者;术后复发或对侧代偿性高分泌的患者。它不仅为无法手术的APA患者提供了微创治愈的可能,也为IHA患者提供了一种深度降压、逆转靶器官损害的有效手段。
结语
从“不可切除”到“精准消融”,从“姑息治疗”到“第三种选择”,董一飞教授的分享为我们勾勒出了一幅高血压介入治疗的未来图景。SAAE技术的崛起,不仅仅是手术方式的革新,更是对PA治疗理念的重构。基于近30年的循证积累与机制深潜,SAAE已具备了成为PA标准治疗方案的底气。随着技术的普及与迭代,我们有理由相信,高血压的介入治疗将进入一个更精准、更微创、更治愈的全新时代。
专家简介
董一飞教授
南昌大学第二附属医院
南昌大学第二附属医院心内科行政副主任,主任医师、教授、博士生导师
日本熊本大学海归博士、博士后
江西省分子医学重点实验室行政副主任
南昌大学第二附属医院难治性高血压诊疗中心执行主任
全国卫生系统青年岗位能手
江西五四青年奖章获得者
江西省百千万人才工程人选
中华医学会心血管病分会青年委员会委员
中国医师协会高血压专业委员会青年委员
中国老年保健协会高血压分会常务委员
中国高血压联盟理事会理事
从事高血压血管病的临床诊治和基础研究。在江西省开创先河,把高血压病的诊治从传统的药物治疗拓展到了微创介入领域,率先在全省开展了原醛症微创介入诊断和治疗技术。主持国家级研究课题4项,省级研究课题6项。在《Hypertension》等期刊发表SCI论文61篇,总影响因子268分,H指数27,他引2614次,发表北大核心中文论文37篇。获国家实用新型专利一项
参考文献:
2.Qiu J, Li N, Xiong HL, et al. Superselective adrenal arterial embolization for primary aldosteronism without lateralized aldosterone secretion: an efficacy and safety, proof-of-principle study. Hypertens Res. 2023 May;46(5):1297-1310.
3.Shuai WL, Zhang HC, Xiong HL, et al. Biochemical Success After Selective Adrenal Arterial Embolization Predicts Long-Term Regression of Aldosterone-mediated Cardiac Remodeling. Am J Hypertens. 2026 Mar 4:hpag015.
4.Lai ZQ, Fu Y, Liu JW, et al. The impact of superselective adrenal artery embolization on renal function in patients with primary aldosteronism: a prospective cohort study. Hypertens Res. 2024 Apr;47(4):944-958.
5.Liang NP, Li N, Wu H,et al. Aldosterone and Impaired Nocturnal Blood Pressure Decline in Primary Aldosteronism. J Am Heart Assoc. 2026 Mar 17;15(6):e044976.
6.Zhang H, Li Q, Liu X, et al. Adrenal artery ablation for primary aldosteronism without apparent aldosteronoma: An efficacy and safety, proof-of-principle trial. J Clin Hypertens (Greenwich). 2020 Sep;22(9):1618-1626.
7.Sun F, Liu X, Zhang H, et al. Catheter-based adrenal ablation: an alternative therapy for patients with aldosterone-producing adenoma. Hypertens Res. 2023 Jan;46(1):91-99.
8.Ji G, Yang C, Hou J, et al. Bilateral adrenal artery embolization for the treatment of idiopathic hyperaldosteronism: A proof-of-principle single center study. Hypertens Res. 2025 Jan;48(1):200-211.

我要留言