编者按:在急性冠脉综合征(ACS)的临床管理中,我们常面临一个棘手的悖论:尽管患者PCI手术获得成功,且在后续随访中使低密度脂蛋白胆固醇(LDL-C)达到指南推荐目标,为何在出院后早期阶段的主要心血管不良事件复发率仍然居高不下?
在中华医学会第二十四次介入心脏病学大会上,哈尔滨医科大学附属第二医院候静波教授带来题为《从ACS诊疗现状来看血脂管理的重要性》的精彩报告,从易损斑块的病理生理本质出发,结合血管内影像学与分子生物学的前沿证据,系统剖析了ACS早期再发事件高发的深层机制,并阐述了早期强化降脂——尤其是他汀联合PCSK9抑制剂——在稳定斑块、阻断炎症通路中的双重获益,为ACS血脂管理的范式转变提供了扎实的理论与循证支撑。

一、临床痛点:ACS易损期事件高发,高危斑块是核心根源
ACS患者出院后一年内再发事件持续处于较高水平,其中急性期后三个月被称为“易损期”,约50%的再发事件集中在这一阶段[1,2](图1)。

图1. ACS患者出院后不同时间段MACE累积发生率对比
影像学研究揭示了再发风险升高的病理基础。ACS患者易损斑块(薄帽纤维粥样斑块,TCFA)比例高达32%,而稳定性冠心病患者仅为3%,相差十倍以上(图2)。更值得警惕的是,ACS患者非罪犯血管与罪犯血管的斑块组成高度相似——这意味着即使成功处理了罪犯病变,其他血管仍存在大量高危斑块,成为再发事件的潜在来源[3]。
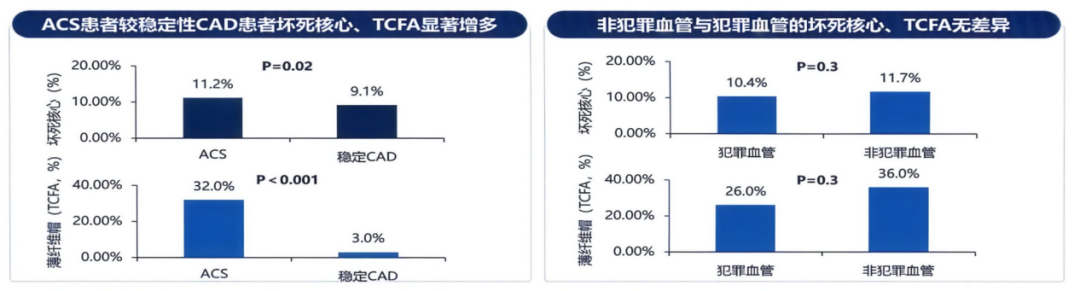
图2. ACS与稳定性冠心病患者罪犯血管/非罪犯血管斑块特征对比
经皮冠状动脉介入治疗(PCI)术后前3个月,正是血管病理愈合与炎症激活的关键阶段,局部缺血事件、斑块进展及不稳定性、全身性缺血事件等多种风险在此阶段均达到峰值[4],术后1年内再次血运重建的风险也持续升高(图3),而滞后的调脂策略无法为患者提供及时有效的保护,进一步放大了早期事件风险。
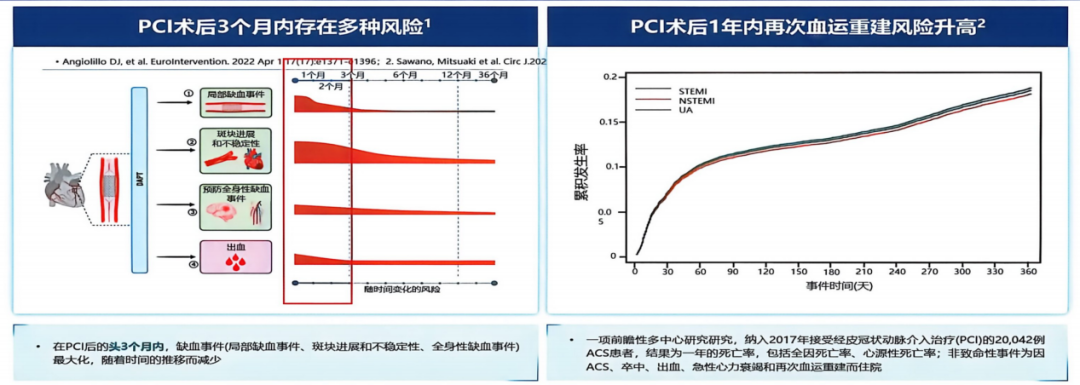
图3. PCI术后随时间变化的缺血风险曲线及1年内再次血运重建风险趋势
二、精准识别高危斑块:量化标准与风险分层
高危斑块即使不造成严重管腔狭窄,仍可能突发破裂导致急性事件。因此,精准识别易损斑块是降低再发事件的关键。
一项由哈尔滨医科大学附属第二医院团队参与的国际多中心OCT随访研究显示[5],临床中超过30%的冠心病患者存在高危斑块特征;4年随访结果表明,存在高危斑块的患者事件发生率达35%,而无高危斑块特征者仅为3.8%,事件风险较无高危斑块者升高约9.4倍,直观印证了高危斑块对患者远期预后的显著影响,也凸显了早期识别并干预的必要性。
基于上述大样本OCT研究,候教授团队进一步将高危斑块的核心特征进行了精准量化[6]。当三个关键量化标准叠加时,事件风险增加15.5倍(图4),其中脂质角度大于225度对风险升高的贡献最为突出。

图4. 三大高危斑块特征及其与心血管不良事件风险关联
基于上述影像学特征,候教授团队2025年发表在《Circulation》杂志的一篇综述提出了基于OCT的高危斑块危险分层策略(图5)[7]。其中,“中危”人群——即高危斑块伴轻中度狭窄者——最易被临床忽略,是ACS再发事件的潜在高风险人群,亟需通过强化药物治疗实现斑块稳定,阻断急性事件链条。
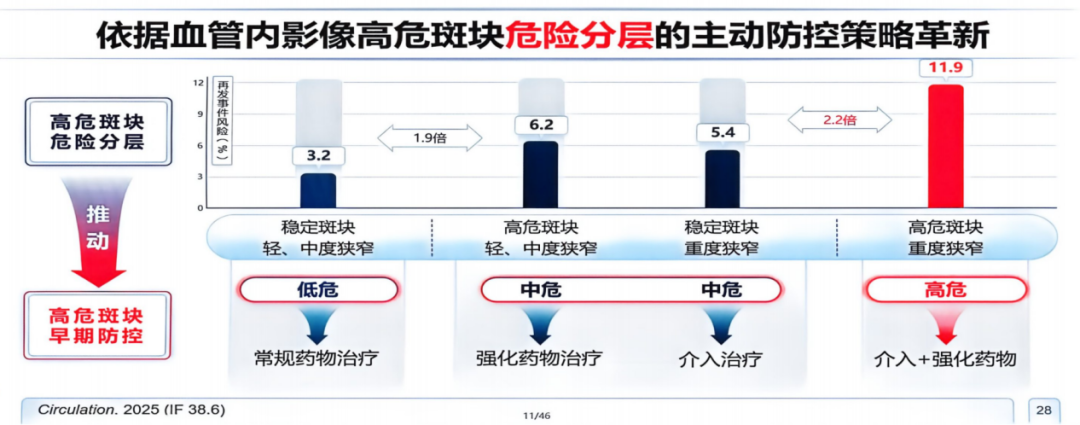
图5. 基于OCT影像的高危斑块危险分层与临床干预策略
三、早期强化降脂的紧迫性与PCSK9的关键作用

传统阶梯式降脂调整周期较长,难以覆盖ACS患者出院后前3个月的关键易损期,常导致风险最高阶段血脂未能及时有效控制。2025年ESC指南及2025年ACC/ACS管理指南均明确提出,ACS患者应在住院期间启动早期、强化、联合的降脂策略,遵循“越早、越低、越好”的原则。指南建议,在最大耐受剂量他汀基础上,若LDL-C仍≥1.8 mmol/L,应联合非他汀类降脂药物;若LDL-C在1.4~1.8 mmol/L之间,也可考虑联合治疗。[2]联合治疗应优选哪一类药物?
为什么PCSK9抑制剂备受关注?候教授从病理机制角度给出了答案。
01
首先,ACS患者PCSK9水平显著升高(图6)[8,9]。更重要的是,他汀在降低LDL-C的同时会反馈性刺激PCSK9转录,导致其水平进一步升高。
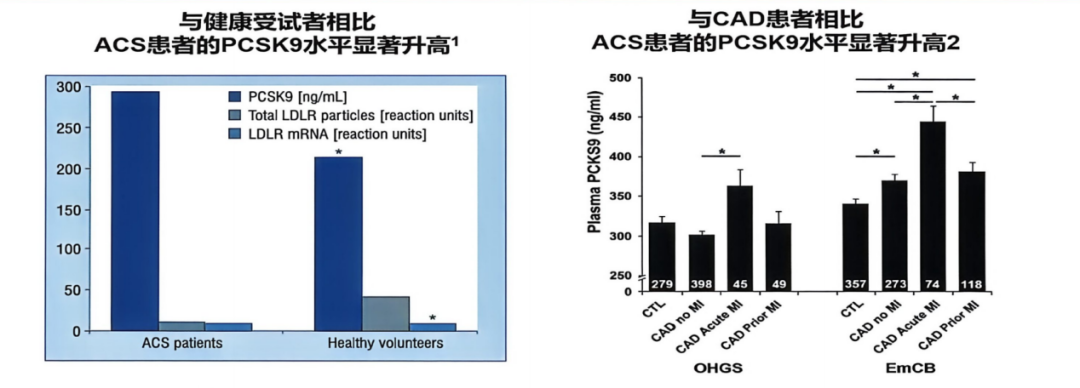
图6. ACS患者与健康人群、稳定性冠心病患者PCSK9水平对比
02
其次,升高的PCSK9并非单纯的伴随现象,而是直接参与斑块不稳定的关键介质。基础研究证实,PCSK9可进入内皮下,与巨噬细胞TLR4受体结合,刺激其吞噬氧化型LDL转化为泡沫细胞,并激活TLR4/NF-κB通路释放大量炎性因子,促进斑块不稳定;此外,PCSK9还可通过旁分泌作用在局部加剧炎症(图7)[10]。
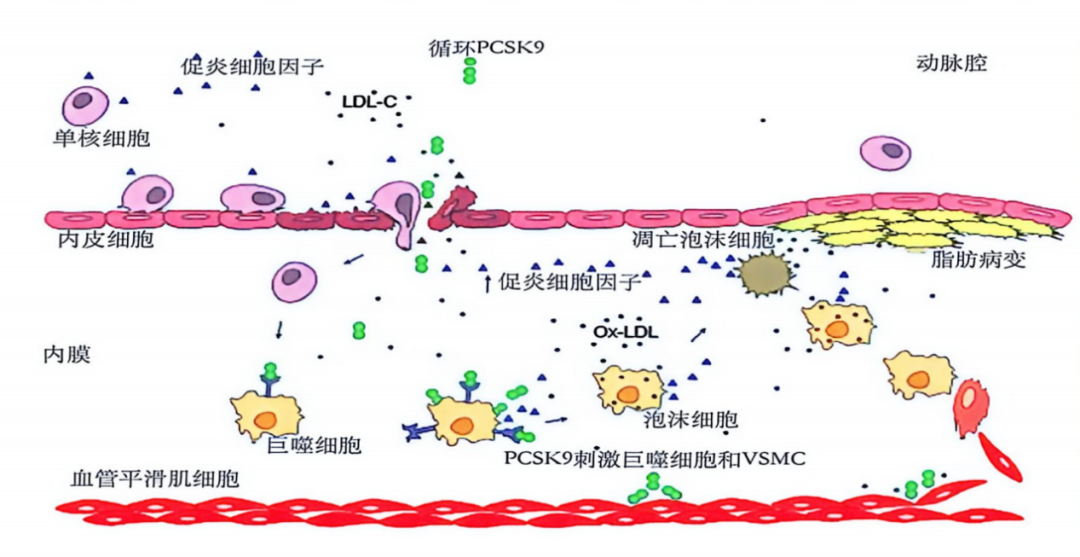
 图7. PCSK9参与斑块炎症与不稳定进程的机制
图7. PCSK9参与斑块炎症与不稳定进程的机制
基于上述机制,候教授提出,ACS早期不稳定阶段在他汀基础上联合PCSK9单抗,可同时阻断肝细胞和斑块局部来源的PCSK9,从而实现快速抗炎、稳定斑块,为降低远期不良事件风险提供核心机制保障。
四、循证证据:早期联合PCSK9抑制剂的多重获益
影像学研究证实,早期联合治疗可实现斑块稳定与逆转。HUYGENS Ⅲ期随机对照研究纳入161例非ST段抬高型急性冠脉综合征患者,结果显示[11],在强化他汀基础上加用依洛尤单抗治疗48周,较安慰剂显著增加最小纤维帽厚度(FCT)21.3 μm(P<0.01),并显著降低斑块体积百分比(PAV)与斑块总体积(TAV)(图8)。
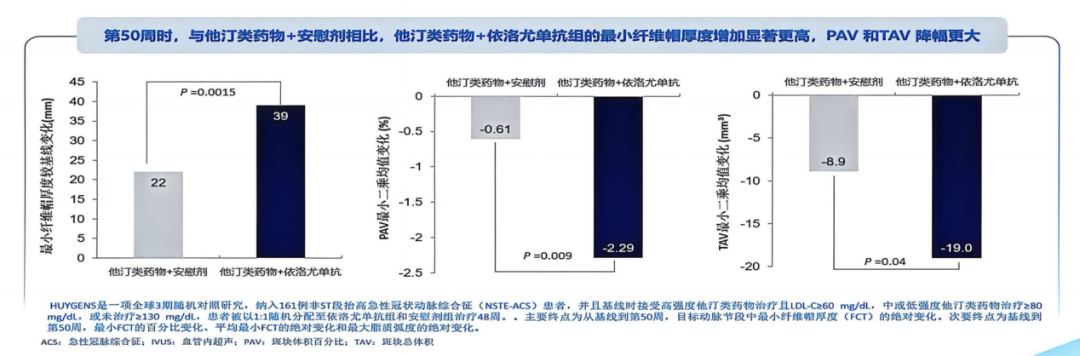
图8. HUYGENS研究中依洛尤单抗与安慰剂组斑块影像学指标变化对比
临床事件研究进一步支持早期达标策略。SWEDEHEART全国队列研究纳入56 262例心梗患者,结果显示[12],心梗后2个月内早期且持续降脂达标者,主要心血管不良事件(MACE)、全因死亡及再发心梗风险显著低于晚期达标或未达标者,呈现“早期优于晚期、持续优于间断”的获益特征(图9)。
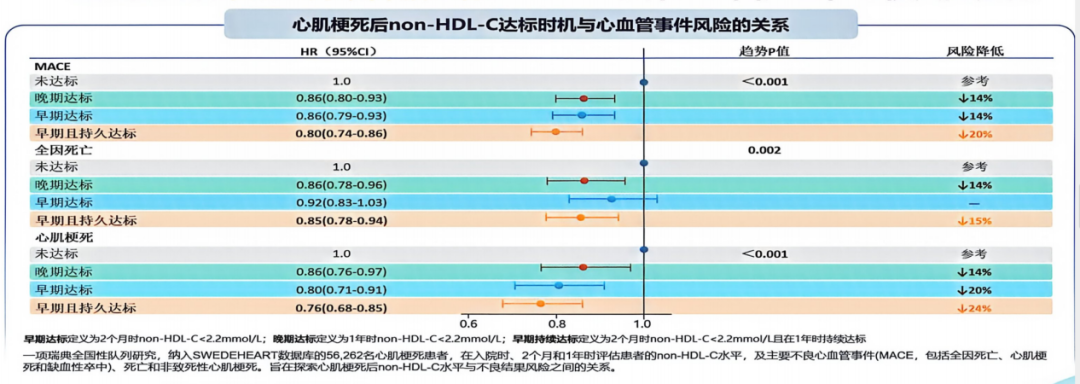
图9. SWEDEHEART研究不同降脂达标时机与心血管事件风险关系
真实世界数据同样验证了院内早期启动的价值。一项基于TriNetX数据库、纳入575 572例急性心肌梗死(AMI)患者的研究显示,发病5天内早期启用PCSK9抑制剂,可显著降低卒中、心衰、恶性心律失常、心脏骤停及死亡等MACE风险(图10),并减少医疗资源消耗[13]。
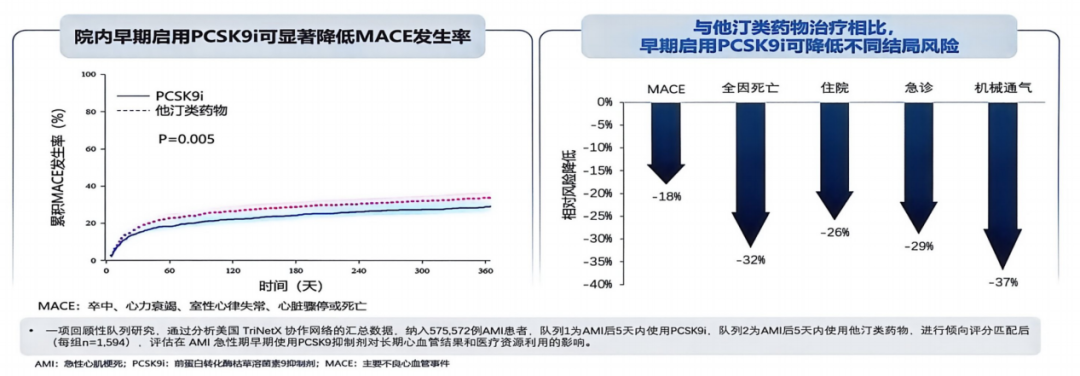
图10. AMI患者院内早期使用PCSK9抑制剂与他汀类药物MACE风险对比
五、长期管理:累积胆固醇暴露与终身风险管理
ACS急性期的强化降脂旨在快速稳定斑块、降低再发事件风险,但斑块管理并非一劳永逸。从长期来看,胆固醇累积暴露量是决定动脉粥样硬化进展与心血管事件的关键因素。
NATURE-PARADOX研究进一步用数据证实,相同累积暴露量下,心血管风险基本一致;而累积暴露量每升高1 mmol/L/年,主要心血管事件风险即显著增加(图11)。这充分说明,动脉粥样硬化性心血管疾病(ASCVD)风险由LDL-C累积暴露量直接决定,因此降脂必须长期维持达标,才能有效控制总体风险[14]。
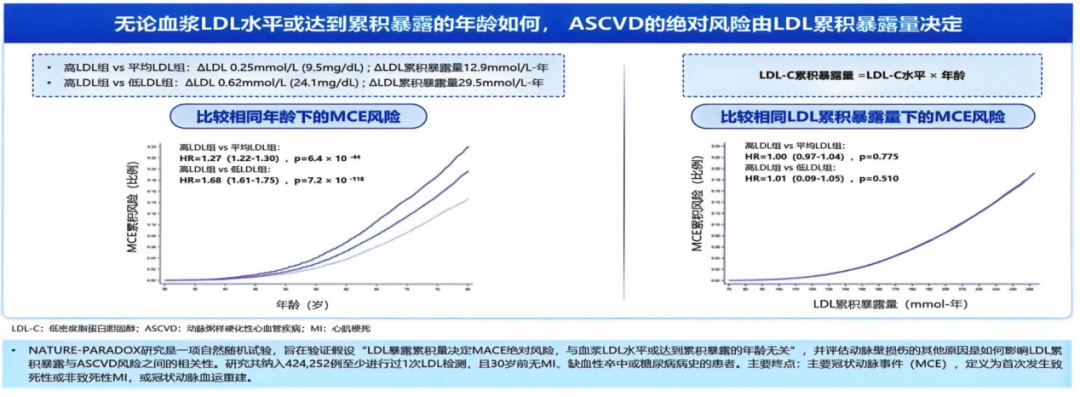
图11. NATURE-PARADOX研究LDL-C累积暴露量与心血管风险关系
这一理念也得到了顶级学术共识的支持。2025年《柳叶刀》委员会建议将“冠状动脉疾病”更名为“动脉粥样硬化性冠状动脉疾病”,标志着临床重心从“处理缺血狭窄”转向“全域干预动脉粥样硬化、早期识别高危斑块”(图12)[15]。这也意味着,降脂干预应尽早启动,并对已有斑块的极高危人群进行严格、长期的血脂管控,实现全程斑块风险控制。
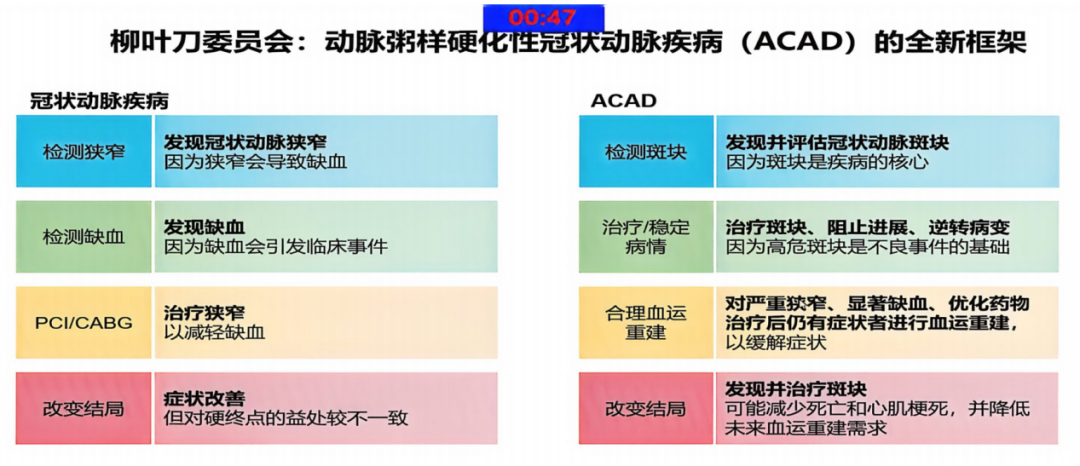
图12. 冠状动脉疾病更名前后诊疗理念对比
小结
ACS血脂管理的关键在于早期干预、强化联合、精准防控、长期坚持:急性期尽早启动他汀联合PCSK9抑制剂,助力快速降脂、抗炎与斑块稳定;通过影像学精准识别高危人群,重点关注易被忽视的中危患者;长期维持血脂达标,控制LDL-C累积暴露,实现全程风险管控。这既是对现有血脂管理策略的优化完善,也推动临床从“关注缺血狭窄”逐步转向“全程干预动脉粥样硬化”,为ACS患者的长期预后提供更全面的保障。
专家简介
候静波教授
哈尔滨医科大学附属第二医院
心血管介入中心主任、心内科副主任,二级教授,主任医师,博士生导师
教育部长江学者特聘教授
寒地心血管病全国重点实验室PI
教育部心肌缺血重点实验室副主任
黑龙江省冠心病与心律失常临床医学研究中心主任
全国五一巾帼标兵获得者,首届龙江名医,获黑龙江省总工会最美女职工称号
中国医师学会心血管分会常委
ISHR中国转化医学第六届委员会常委
中华医学会心血管病分会介入学组副组长
黑龙江省老年医学学会心血管病专业委员会主任委员
黑龙江省医学会心血管专业委员会副主任委员
黑龙江省医师协会心血管内科专业委员会副主任委员
黑龙江省心脏学会副会长;FACC,FSCAI等。
参考文献:
2.Chi G, Lee JJ, Kazmi SHA, et al. Early and late recurrent cardiovascular events among high-risk patients with an acute coronary syndrome: Meta-analysis of phase III studies and implications on trial design. Clin Cardiol. 2022 Mar;45(3):299-307.
3.Pundziute G, Schuijf JD, Jukema JW, et al. Evaluation of plaque characteristics in acute coronary syndromes: non-invasive assessment with multi-slice computed tomography and invasive evaluation with intravascular ultrasound radiofrequency data analysis. Eur Heart J. 2008 Oct;29(19):2373-81.
4.Angiolillo DJ, Galli M, Collet JP, et al. Antiplatelet therapy after percutaneous coronary intervention. EuroIntervention. 2022 Apr 1;17(17):e1371-e1396.
5.Xing L, Higuma T, Wang Z, et al. Clinical Significance of Lipid-Rich Plaque Detected by Optical Coherence Tomography: A 4-Year Follow-Up Study. J Am Coll Cardiol. 2017 May 23;69(20):2502-2513.
6.Jiang S, Fang C, Xu X, Xing L, et al. Identification of High-Risk Coronary Lesions by 3-Vessel Optical Coherence Tomography. J Am Coll Cardiol. 2023 Apr 4;81(13):1217-1230.
7.Dai J, Zhao J, Xu X, et al. Long-Term Prognostic Implications of Non-Culprit Lesions in Patients Presenting With an Acute Myocardial Infarction: Is It the Angiographic Stenosis Severity or the Underlying High-Risk Morphology? Circulation. 2025 Apr 15;151(15):1098-1110.
8.Burchardt P, Rze?niczak J, Dudziak J, et al. Evaluation of plasma PCSK9 concentrations, transcript of LDL receptor, as well as the total number of monocyte LDL receptors in acute coronary syndrome patients. Cardiol J. 2016;23(6):604-609.
9.Almontashiri NA, Vilmundarson RO, Ghasemzadeh N, et al. Plasma PCSK9 levels are elevated with acute myocardial infarction in two independent retrospective angiographic studies. PLoS One. 2014 Sep 2;9(9):e106294.
10.Punch E, Klein J, Diaba-Nuhoho P, et al. Effects of PCSK9 Targeting: Alleviating Oxidation, Inflammation, and Atherosclerosis. J Am Heart Assoc. 2022 Feb;11(3):e023328.
11.Nicholls SJ, Kataoka Y, Nissen SE, et al. Effect of Evolocumab on Coronary Plaque Phenotype and Burden in Statin-Treated Patients Following Myocardial Infarction. JACC Cardiovasc Imaging. 2022 Jul;15(7):1308-1321.
12.Schubert J, Leosdottir M, Lindahl B, et al. Intensive early and sustained lowering of non-high-density lipoprotein cholesterol after myocardial infarction and prognosis: the SWEDEHEART registry. Eur Heart J. 2024 Oct 14;45(39):4204-4215.
13.Chao T H , Lee Y C , Wang S I ,et al.Early PCSK9 inhibitor subscription during episode of acute myocardial infarction (EPISODE-AMI) study[J].European Heart Journal, 2025(Supplement_1):Supplement_1.
14.2023?ESC?congress:?NATURE-PARADOX: Naturally Randomized Trial of Titrating Cumulative Exposure to LDL to Solve the Prevention Paradox
15.Zaman S, Wasfy JH, Kapil V, et al. The Lancet Commission on rethinking coronary artery disease: moving from ischaemia to atheroma. Lancet. 2025 Apr 12;405(10486):1264-1312.


我要留言