编者按:
肾动脉去神经术(RDN)的出现,为高血压治疗开辟了继生活方式干预和药物治疗之后的第三条路径。然而,RDN在临床实践中仍面临一个核心挑战:应答率有限。如何突破这一瓶颈?近日,在“中华医学会第二十四次介入心脏病学大会(CIT2026)”上,中国医科大学附属第一医院孙国哲教授代表孙英贤主任和重庆医科大学附属第二医院殷跃辉主任团队系统介绍了电刺激标测技术及临床实践策略,探讨如何通过精准定位技术提升RDN的治疗效果。

血压调控的神经密码:交感与副交感的平衡之道
血压的稳态维持,依赖于交感神经与副交感神经的精细协同。交感神经如同“油门”,其兴奋可增快心率、收缩血管、激活肾素-血管紧张素-醛固酮系统(RAAS),从而升高血压;而副交感神经(主要通过迷走神经)则扮演“刹车”角色,减慢心率、促进血管舒张,发挥降压效应。两者相互拮抗、动态平衡,共同维系血压在正常范围内。
在高血压患者中,这一平衡被打破——交感神经过度激活成为主导。研究表明,高血压患者的肌肉交感神经活性显著高于血压正常人群,动静脉儿茶酚胺水平也明显升高。过度兴奋的交感神经通过传出纤维促进肾素释放、增加钠水重吸收、减少肾血流量;同时通过传入纤维将升压信号传递至中枢,进一步强化全身交感输出,形成恶性循环。
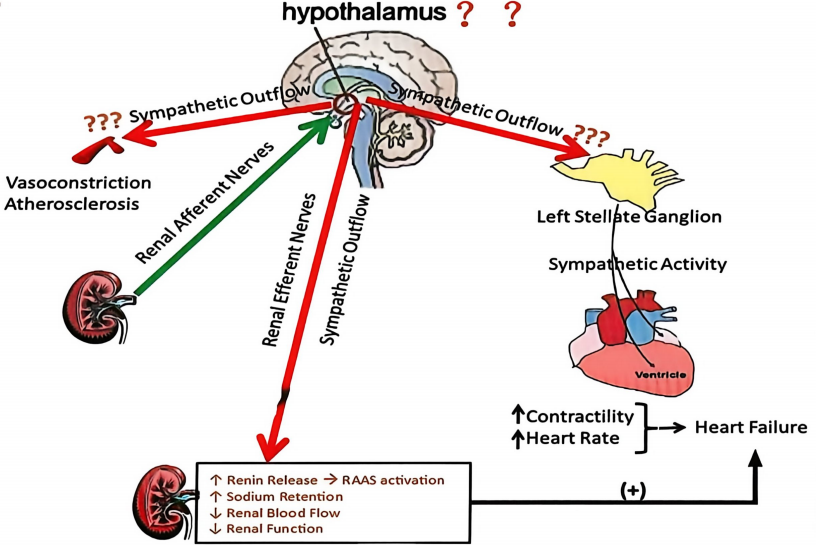
图1. 交感神经过度激活介导高血压的病理生理机制
RDN的核心理念是纠正交感-副交感的失衡——适度阻断过度活跃的交感信号,同时保留副交感的正常调节功能。因此,实现这一目标的关键在于精准定位交感神经,以区分“应消融”的交感优势位点与“应保护”的副交感优势位点。
相互交错的神经网络,复杂的肾神经分布
然而,肾动脉周围的神经网络并非单一、有序的结构,而是交感神经与副交感神经相互交错、混杂分布的复杂网络,使得精准定位面临巨大挑战。
组织学研究发现,约90.5%的神经位于肾动脉管腔2.0 mm范围内,其中既有交感纤维,也有副交感纤维,且两者的比例在不同节段、不同位点差异显著。神经数量从肾动脉近端到远端逐渐增多(近端216条 → 远端417条),分布极不均衡[1]。
这意味着,同样是肾动脉周围的一个点,其神经构成可表现为交感为主、副交感为主或二者混合。不加区分地进行地毯式消融,必然面临误伤的风险。
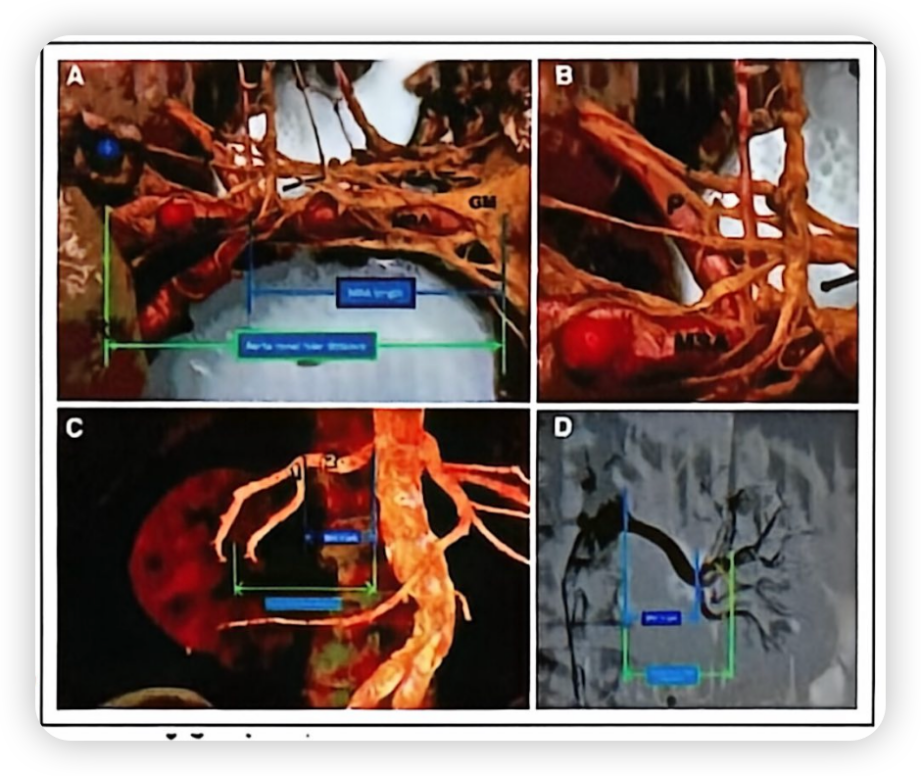
图2. 肾周神经网络
“盲消”的困境:为什么消了,血压不降反升?
早期RDN正是采用了这种“盲消”策略——无论神经类型、不分位点优劣,对肾动脉周围进行全面消融。然而临床数据显示:即使采用主干+分支联合消融,仍有25%~30%的患者血压无明显下降,少数患者甚至出现血压升高[2]。
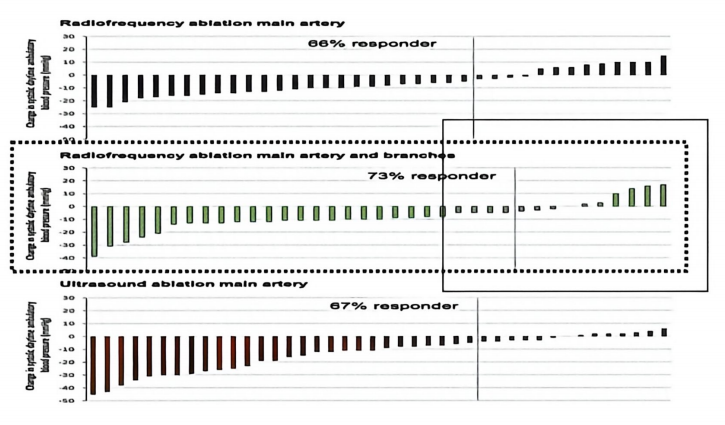
图3. 不同RDN消融策略的血压应答对比
原因并不复杂:如果消融的是交感优势位点,可有效降压;但如果误伤了副交感优势位点,相当于拆除了天然的“刹车”机制,反而可能导致血压升高。
这就是“盲消”的根本缺陷——不分敌友,一律消灭。而要突破这一困境,逻辑上只有一条路:消融之前,先看清位点的神经属性。
破局之道:电刺激标测,让神经“开口说话”
如何判断一个位点是“敌”是“友”?基于肾神经电刺激(RNS)的标测技术提供了解决方案。其原理是:对肾动脉某一位点施加电刺激,同时观察即时血压反应:如果血压升高,提示该位点以交感神经为主,可进行消融;如果血压降低,提示该位点以副交感神经为主,应避免消融。
通过这种“刺激-反应-判断-消融-验证”的闭环流程,术者可以精准识别交感优势位点,保护副交感神经,进而提高RDN应答率,减少无效消融和并发症。
基于动物实验的观察,电刺激后的血压反应可分为以下五种类型[3]:
1型:表现为血压持续升高并稳定于基线之上,代表该位点交感神经占绝对优势,强烈建议消融;
2型:表现为血压先下降后上升且最终超过基线水平,代表交感神经占相对优势,建议消融;
3型:表现为血压先下降后上升但未超过基线,代表副交感神经占相对优势,不建议消融;
4型:表现为血压在基线附近波动,提示该位点无神经或为混合型,不值得消融;
5型:表现为血压持续降低并稳定于基线之下,代表副交感神经占绝对优势,禁止消融。
那么,这一分型是否真正对应了不同的消融结局?换言之,按照上述原则“该消的消、该避的避”,能否带来预期的降压效果?研究对此进行了验证:
升压点(对应1型、2型):刺激后血压升高,消融后血压可下降约10 mmHg;
降压点(对应5型):刺激后血压下降,消融后血压反而可能升高;
无反应点(对应4型):消融效果不明确,且可能增加血管损伤风险。
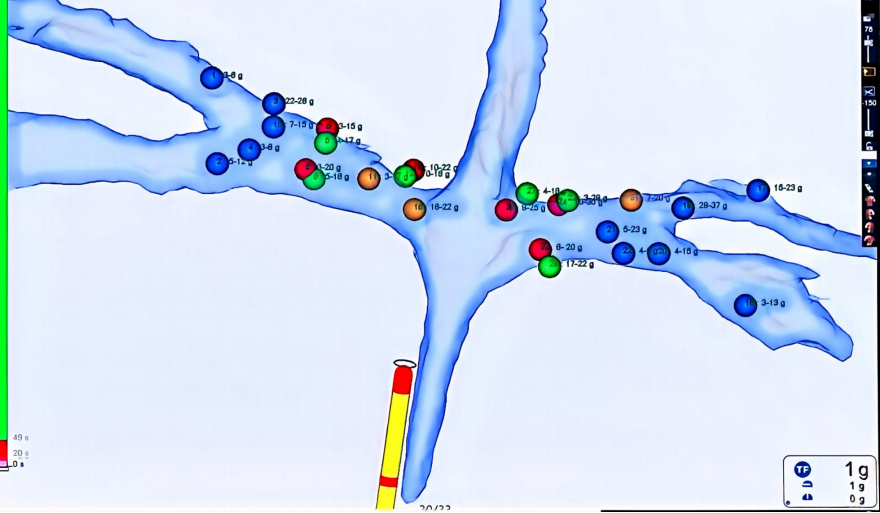
图4. RNS标测指导的精准RDN消融
研究还发现,电刺激后血压升高幅度越高的位点,消融后血浆去甲肾上腺素水平和血压降低越明显;而血压升高幅度较低的位点则效果相对较弱。
综上,电刺激标测不仅能够帮助术者在消融前“看清”位点的神经属性,还能通过反应类型和幅度预测消融后的降压效果。
临床实践:如何实施精准消融?

那么,这一精准策略在临床实践中如何落地?基于上述电刺激标测原理及临床研究验证,精准RDN的手术流程可归纳如下:
Step 1. 建立通路:经股动脉或桡动脉将标测导管送至肾动脉远端;
Step 2. 逐点电刺激:从远端向近端逐点释放电刺激(参数通常为20 Hz、2 ms),以激发该位点的神经反应;
Step 3. 判断位点类型:根据刺激后血压波形的变化,根据前文所述的五种分型标准进行判断;
Step 4. 精准消融:仅对1型和2型位点进行消融,对5型位点严格禁止消融,对3型和4型位点则不建议消融;
Step 5. 验证效果:消融后再次电刺激,确认升压效应是否消失,以验证消融效果。
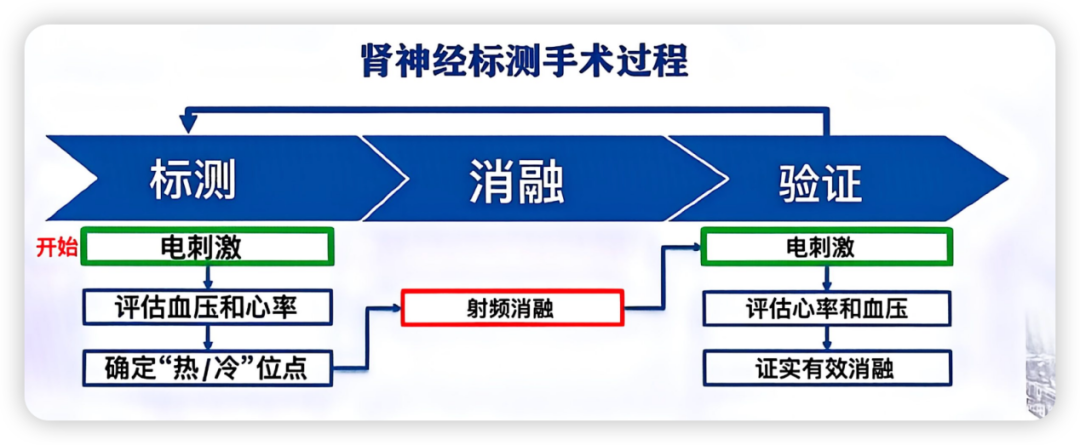
图5. 肾神经标测手术过程
通过这一“刺激-判断-消融-验证”的闭环流程,RDN可显著提高治疗应答率,避免无效消融和副交感损伤,为难治性高血压患者提供更安全、更有效的介入治疗方案。
结语
RDN的发展历程,是一部从经验走向循证、从盲消走向精准的技术进化史。早期以“主干+分支联合消融”为代表的解剖消融策略,虽已获得指南推荐,但应答率不佳的根源在于对副交感优势位点的误伤。
电刺激标测技术的出现,为这一困境提供了破局之道。通过“刺激-判断-消融-验证”的闭环流程,术者能够在消融前精准识别位点的神经属性:区分“敌友”,打击交感优势位点,保护副交感优势位点,回避无效位点。研究证实,这一精准策略可有效避免无效消融和血管损伤。
展望未来,随着标测技术的不断优化和新型消融导管的迭代,个体化、精准化的RDN治疗将成为难治性高血压介入治疗的新常态,为更多患者带来安全、有效的降压获益。
专家简介
孙英贤 教授
中国医科大学附属第一医院
主任医师,二级教授,博士研究生导师
中国医科大学附属第一医院 心内科主任
中国医科大学心血管研究所所长、内科学科带头人
国际欧亚科学院院士
中华医学会心血管病分会 副主任委员
中国医师协会高血压专业委员会 主任委员
中华医学会内科学分会 副主任委员
辽宁省医师协会内科医师分会 会长
Asian Heart Journal 主编
Journal of Translational Internal Medicine(SCI收录)副主编
殷跃辉 教授
重庆医科大学附属第二医院
主任医师,二级教授,博士生导师,国务院特殊津贴专家
欧洲心脏病学会、欧洲心律学会和亚太心律学会资深委员
重庆市心血管病学学术技术带头人
重庆市心律失常介入诊疗质量控制中心主任
国家心律失常介入培训基地主任
重庆市卫生局心律失常重点研究室主任
中华医学会心电生理和起搏分会常务委员
中国医师协会心律学专委会委员
中国生物医学工程学会心律学分会委员
中国房颤联盟副主席
中国高血压介入治疗工作委员会副主任委员
中国心电技术学会委员
重庆市心脏起搏与心电生理学会前任主任委员
重庆医师协会心律学专委会主任委员
重庆市医学会心血管病学分会副主委
从医39年来,潜心致力于临床心脏电生理研究,在快速性心律失常的导管消融治疗,特别是疑难复杂快速性心律失常的标测与导管消融方面造诣精深,在RDN治疗顽固性高血压及心力衰竭等方面有深入的研究,处于世界先进水平。
在国际顶级刊物上发表SCI论文103篇。获得国家发明专利2项,实用新型专利5项,承担国家自然科学基金4项。参编专著5部,转化临床创新项目2项。
2006年发表在欧洲心脏杂志(European Heart Journal)的论文被引97次,并被2010年的欧洲房颤指南引用,这是我国心律失常领域的研究成果首次被国际权威的房颤指南所引用。
擅长:心血管领域的常见病的诊断和治疗;常见心律失常和复杂心律失常的诊断和治疗;冠心病的诊断和介入治疗;高血压的药物和介入治疗;心血管疾病的临床研究。
孙国哲 教授
中国医科大学附属第一医院
教授、主任医师 博士研究生导师
中国医科大学附属第一医院心血管内科病区副主任
“兴辽英才计划”青年拔尖人才,沈阳市领军人才,中国医科大学青年拔尖人才
中华医学会心血管病学分会动脉粥样硬化与冠心病学组副组长
辽宁省细胞生物学学会心血管疾病医工融合专业委员会主任委员
中国医药教育协会高血压专业委员会副主任委员
辽宁省医学会心血管病学分会委员
科研课题:主持十四五国家科技重大专项课题1项、国家自然科学基金1项、辽宁省科学技术计划项目1项、辽宁省自然科学基金1项、辽宁省教育厅高校基本科研项目1项。
以第一/通讯作者(含共同作者)在Lancet、Nature Medicine、JAMA Cardiology、Lancet Reg Health West Pac、JAMA Netw Open 等发表SCI论文35篇
荣获辽宁省科技进步一等奖2项、辽宁杰出科技青年奖(十大英才)
主要方向:高血压及人群心血管防控、冠脉和高血压介入治疗
参考文献1.Hypertension. 2020;76:1240-1246. DOI: 10.11612.Bhatt DL, Kandzari DE, O'Neill WW, et al. A controlled trial of renal denervation for resistant hypertension. N Engl J Med. 2014;370(15):1393-1401.3. Zhou H, Li Y, Xu Y, et al. Mapping renal innervations by renal nerve stimulation and characterizations of blood pressure response patterns. J Cardiovasc Transl Res. 2021.

我要留言